
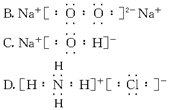
科目:高中化学 来源:不详 题型:单选题
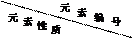 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||
| 原子半径/10-10 m | 0.66 | 1.36 | 1.23 | 1.10 | 0.99 | 1.54 | 0.70 | 1.18 | |||||||||||
| 最高或最低化合价 | | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |||||||||||
| -2 | | | -3 | -1 | | -3 |
查看答案和解析>> 科目:高中化学 来源:不详 题型:填空题 A+、B+、C-、D、E五种粒子(分子或离子)中每个粒子均有10个电子,已知:①A++C-====D+E↑;②B++C-====2D。请回答: (1)C-的电子式是_____________________。 (2)具有相同空间构型的粒子是____________和____________。 (3)写出B+和E反应的离子方程式:________________________________________________。 查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 判断下列说法中不正确的是( ) A.具有离子键的化合物一定是离子化合物 B.由一种元素的阳离子和另一种元素的阴离子构成的物质一定是纯净物 C.A、B两种单核离子所带的电性和电荷数相同,离子的核外电子层数也相同,则A、B一定为同种元素的原子 D.两种离子化合物AX3和AX2的水溶液,AX3的氧化性较AX2的强 查看答案和解析>> 科目:高中化学 来源:不详 题型:填空题 有A、B、C、D四种不同元素的原子,A、C、D具有相同的电子层数,A的M层比C的M层多4个电子,比D的M层少2个电子,B的L层比A的L层少3个电子。画出A、B、C、D的原子结构示意图。 查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 下列 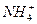 与NH3所含的质子数、核外电子数的关系描述正确的是( ) 与NH3所含的质子数、核外电子数的关系描述正确的是( )
查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 Na2O2、CaC2、CaH2、FeS2均为离子化合物,前三种物质极易与水反应。下列叙述正确的是( )
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |