
分析 可假设原溶液的质量为mg,根据溶液稀释前后溶质的质量不变计算m,根据质量分数计算NaNO3的质量,根据n=$\frac{m}{M}$计算NaNO3的物质的量,再根据c=$\frac{n}{V}$计算.
解答 解:设原溶液的质量为mg,
则根据溶液稀释前后溶质的质量不变,则m×22%=(m+100)×14%,解之得m=175,
则在150mL溶质的质量分数为22%的NaNO3溶液中,含NaNO3的质量为175×22%=38.5g,
NaNO3的物质的量为$\frac{38.5g}{85g/mol}$=0.45mol,
原溶液的物质的量浓度是$\frac{0.45mol}{0.15L}$=3mol/L,
故答案为:3mol/L.
点评 本题考查物质的量浓度计算,侧重考查分析计算能力,明确稀释前后溶质不变是解本题关键,熟练掌握物质的量有关公式,题目难度不大.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:选择题
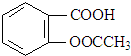
| A. | 阿司匹林的分子式为C9H8O4 | |
| B. | 阿司匹林苯环上的一氯取代物有2种 | |
| C. | 阿司匹林能与NaHCO3溶液反应,最多能与5 mol H2发生加成反应 | |
| D. | 1 mol 阿司匹林与足量NaOH溶液反应,最多消耗NaOH的量为2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸烟有害健康 | |
| B. | 尼古丁中C、H、N三种元素的质量比为5:7:1 | |
| C. | CO比O2更易同血红蛋白结合,会导致人体缺氧 | |
| D. | 尼古丁中氮元素的质量分数约为17.3% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z-+H2O═HZ+OH- | B. | HY+H2O═H3O++Y- | ||
| C. | 常温下,电离度:HX>HY>HZ | D. | HX+Z-→X-+HZ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
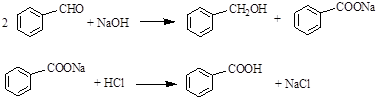
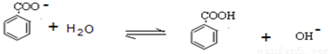 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com