
一定温度下,10 mL 0.40 mol·L-1 H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6 min的平均反应速率:
v(H2O2)≈3.3×10-2 mol·L-1·min-1
B.6~10 min的平均反应速率:
v(H2O2)<3.3×10-2 mol·L-1·min-1
C.反应到6 min时,c(H2O2)=0.30 mol·L-1
D.反应到6 min时,H2O2分解了50%
答案 C
解析 2H2O2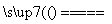 2H2O+O2↑A项,6 min时,生成O2的物质的量n(O2)=
2H2O+O2↑A项,6 min时,生成O2的物质的量n(O2)=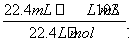 =1×10-3 mol,依据反应方程式,消耗n(H2O2)=2×10-3 mol,所以0~6 min时,v(H2O2)=
=1×10-3 mol,依据反应方程式,消耗n(H2O2)=2×10-3 mol,所以0~6 min时,v(H2O2)=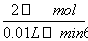 ≈3.3×10-2 mol·L-1·min-1,正确;B项,6~10 min时,生成O2的物质的量n(O2)=
≈3.3×10-2 mol·L-1·min-1,正确;B项,6~10 min时,生成O2的物质的量n(O2)=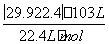 ≈0.335×10-3 mol,依据反应方程式,消耗n(H2O2)=0.335×10-3 mol×2=0.67×10-3 mol,6~10 min时,v(H2O2)=
≈0.335×10-3 mol,依据反应方程式,消耗n(H2O2)=0.335×10-3 mol×2=0.67×10-3 mol,6~10 min时,v(H2O2)=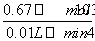 ≈1.68×10-2 mol·L-1·min-1<3.3×10-2 mol·L-1·min-1,正确;C项,反应至6 min时,消耗n(H2O2)=2×10-3 mol,剩余n(H2O2)=0.40 mol·L-1×0.01 L-2×10-3 mol=2×10-3 mol,c(H2O2)=
≈1.68×10-2 mol·L-1·min-1<3.3×10-2 mol·L-1·min-1,正确;C项,反应至6 min时,消耗n(H2O2)=2×10-3 mol,剩余n(H2O2)=0.40 mol·L-1×0.01 L-2×10-3 mol=2×10-3 mol,c(H2O2)= =0.20 mol·L-1,错误;D项,反应至6 min时,消耗n(H2O2)=2×10-3 mol,n(H2O2)总=4×10-3 mol,所以H2O2分解了50%,正确。
=0.20 mol·L-1,错误;D项,反应至6 min时,消耗n(H2O2)=2×10-3 mol,n(H2O2)总=4×10-3 mol,所以H2O2分解了50%,正确。


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)Ca(OH)2能制成澄清石灰水,所以可配制2.0 mol·L-1的Ca(OH)2溶液( )
(2014·广东理综,9D)
(2)溶解度小的沉淀易向溶解度更小的沉淀转化,所以ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀( )
(2014·安徽理综,12D)
(3)验证Fe(OH)3的溶解度小于Mg(OH)2,可将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色( )
(2014·四川理综,4D)
(4)25 ℃时Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度( )
(2014·重庆理综,3D)
(5)AgCl沉淀易转化为AgI沉淀且K(AgX)=c(Ag+)·c(X-),故K(AgI)<K(AgCl)( )
(2013·重庆理综,2D)
(6)CaCO3难溶于稀硫酸,也难溶于醋酸( )
(2013·天津理综,5B)
(7)饱和石灰水中加入少量CaO,恢复至室温后溶液的pH不变( )
(2012·重庆理综,10C)
(8)在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大( )
(2012·天津理综,5B)
(9)AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同( )
(2010·天津理综,4C)
查看答案和解析>>
科目:高中化学 来源: 题型:
( 在5-氨基四唑(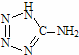 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
(1)基态Ga原子的电子排布式可表示为 ;
(2)5-氨基四唑中所含元素的电负性由大到小的顺序为 ;
在1mol 5-氨基四唑中含有的σ键的数目为 。
(3)叠氮酸钠(NaN3)是传统家用汽车安全气囊中使用的气体发生剂。
①叠氮酸钠(NaN3)中含有叠氮酸根离子(N3-),根据等电子体原理N3-的空间构型为 。②以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化钛化合物。其结构是用碳原子取代氮化钛晶胞(结构如上图示)顶点的氮原子,这种碳氮化钛化合物的化学式为 。
③与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的元素有 。(填写元素符号)
④ [Ti(OH)2(H2O)4]2+中的化学键有 。
A.σ键 B.π键 C.离子键 D.配位键

查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应4CO+2NO2N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A.v(CO)=1.5 mol·L-1·min-1
B.v(NO2)=0.7 mol·L-1·min-1
C.v(N2)=0.4 mol·L-1·min-1
D.v(CO2)=1.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法中一定不正确的是( )
| 组别 | 对应曲线 | c(HCl)/mol·L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |
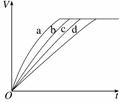
A.第4组实验的反应速率最慢
B.第1组实验中盐酸的浓度大于2.5 mol·L-1
C.第2组实验中盐酸的浓度等于2.5 mol·L-1
D.第3组实验的反应温度低于30 ℃
查看答案和解析>>
科目:高中化学 来源: 题型:
催化反硝化法可用于治理水中硝酸盐的污染,H2能将NO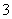 还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12,上述反应的离子方程式为________________________________________________________________________
还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12,上述反应的离子方程式为________________________________________________________________________
________________________________________________________________________,
其平均反应速率v(NO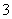 )为________ mol·L-1·min-1。
)为________ mol·L-1·min-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用锌粒与V mL浓度为10%的稀硫酸反应制取氢气,若向反应混合物中加入下列物质,关于反应速率v说法正确的是( )
A.少量Na2SO4固体,v(H2)减小
B.V mL BaCl2溶液,v(H2)不变
C.加入细小的碳粒,v(H2)增大
D.加入NH4HSO4固体,v(H2)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
H2CO3的电离平衡常数Ka1=4.3×10-7,Ka2=5.6×10-11,它的Ka1、Ka2差别很大的原因(从电离平衡的角度解释):_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、SiO2等杂质。利用钛铁矿制备二氧化钛,进一步制备钛单质,流程如图:
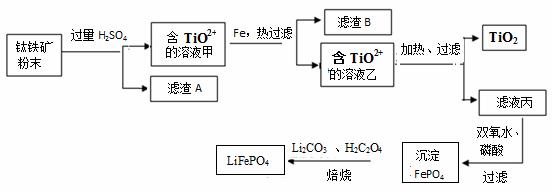
已知:FeTiO3+4H+=Fe2++TiO2++2H2O
草酸(C2H2O4)具有很强还原性,易被氧化成二氧化碳
(1)化合物FeTiO3中铁元素的化合价是 。
(2)钛铁矿加入过量H2SO4后,得到的滤渣A为_______________(填化学式)。
(3)含TiO2+ 溶液乙转化生成TiO2的离子方程式是 。
(4)由滤液丙制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是 。
(5)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。滴定分析时,称取TiO2(摩尔质量为M g/mol)试样w g,消耗c mol/L NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数为 (用代数式表示)。

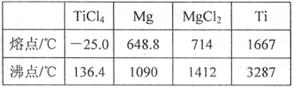 (6)TiO2制取单质Ti,涉及到的步骤如下:
(6)TiO2制取单质Ti,涉及到的步骤如下:
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
反应②的方程式是 , 由TiCl4→Ti需要在Ar气中进行的理由是 。反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据表中信息,需加热的温度略高于 ℃即可。
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com