
½šŹō¼üµÄŠĪ³ÉŹĒĶعż(””””)
A£®½šŹōŌ×ÓÓė×ŌÓɵē×ÓÖ®¼äµÄĻą»„×÷ÓĆ
B£®½šŹōĄė×ÓÓė×ŌÓɵē×ÓÖ®¼äĒæĮŅµÄĻą»„×÷ÓĆ
C£®×ŌÓɵē×ÓÖ®¼äµÄĻą»„×÷ÓĆ
D£®½šŹōĄė×ÓÖ®¼äµÄĻą»„×÷ÓĆ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹ŲÓŚSiO2¾§ĢåµÄŠšŹöÕżČ·µÄŹĒ(NA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄŹżÖµ)(””””)
A£®Ķس£×“æöĻĀ£¬60gSiO2¾§ĢåÖŠŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA
B£®60gSiO2¾§ĢåÖŠŗ¬ÓŠ2NAøöSi”ŖO¼ü
C£®¾§ĢåÖŠÓėĶ¬Ņ»¹čŌ×ÓĻąĮ¬µÄ4øöŃõŌ×Ó“¦ÓŚĶ¬Ņ»ĖÄĆęĢåµÄ4øö¶„µć
D£®SiO2¾§ĢåÖŠŗ¬ÓŠ1øö¹čŌ×Ó£¬2øöŃõŌ×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¹ŲÓŚ½šŹō¾§ĢåµÄĖµ·ØÖŠ²»ÕżČ·µÄŹĒ(””””)
A£®½šŹō¾§ĢåÖŠŅ»¶Ø“ęŌŚ½šŹō¼ü
B£®½šŹō¾§ĢåÖŠµÄ½šŹō¼üƻӊ·½ĻņŠŌŗĶ±„ŗĶŠŌ
C£®½šŹō¾§ĢåÖŠ½šŹōŌ×ÓÖ»ÄܲÉČ”×īĆܶѻż·½Ź½ŠĪ³É¾§Ģå
D£®½šŹō¾§ĢåÖŠµÄ×ŌÓɵē×ÓĪŖÕūøö½šŹōĖł¹²ÓŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠÓŠ¹Ų¾§ĢåµÄĖµ·ØÕżČ·µÄŹĒ(””””)
A£®¾§°ūŹĒ¾§Ģå½į¹¹µÄ×īŠ”ÖŲø“µ„ŌŖ
B£®A2ŠĶ×īĆܶѻż³ĘĪŖĮł·½×īĆܶѻż
C£®NaCl¾§ĢåÖŠCl£ĢīŌŚNa£«ĖłŠĪ³ÉµÄæÕĻ¶ÖŠ
D£®ZnS¾§ĢåÖŠµÄS2£°“A3ŠĶ·½Ź½½ųŠŠ×īĆܶѻż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
»ÆŗĻĪļYX2”¢ZX2ÖŠX”¢Y”¢Z¶¼ŹĒĒ°ČżÖÜĘŚŌŖĖŲ£¬XÓėYĶ¬ÖÜĘŚ£¬YÓėZĶ¬Ö÷×壬YŌŖĖŲŌ×Ó×īĶā²ćµÄp¹ģµĄÖŠµÄµē×ÓŹżµČÓŚĒ°Ņ»µē×Ó²ćµÄµē×Ó×ÜŹż£¬XŌ×Ó×īĶā²ćµÄp¹ģµĄÖŠÓŠŅ»øö¹ģµĄĢī³äĮĖ2øöµē×Ó”£
(1)XŌ×ӵĵē×ÓÅŲ¼Ź½ŹĒ______________£»YŌ×ӵļŪ²ćµē×Ó¹ģµĄ±ķŹ¾Ź½ŹĒ__”£
(2)YX2µÄ·Ö×Ó¹¹ŠĶŹĒ____________£¬YX2µÄČÜ”¢·Šµć±ČZX2________(Ģī”°øß”±»ņ”°µĶ”±)£¬ĄķÓÉŹĒ____________________________________”£
(3)YX2·Ö×ÓÖŠ£¬YŌ×ÓµÄŌÓ»ÆĄąŠĶŹĒ________”£YX2·Ö×ÓÖŠŗ¬________øö¦Š¼ü”£
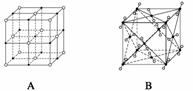
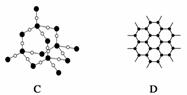
(4)ĻĀĶ¼±ķŹ¾Ņ»Š©¾§ĢåµÄ½į¹¹(¾§°ū)£¬ĘäÖŠ“ś±ķYX2µÄŹĒ____________(ĢīŠņŗÅ£¬ĻĀĶ¬)£¬“ś±ķZX2µÄŹĒ____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¼ų±š¾§Ģå×īæÉææµÄæĘѧ·½·ØŹĒ(””””)
A£®²ā¶ØČŪ”¢·Šµć B£®¹Ū²ģĶāŠĪ
C£®XÉäĻßŃÜÉä D£®±Č½ĻÓ²¶Č
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚ40 kPaøßŃ¹ĻĀ£¬ÓĆ¼¤¹āĘ÷¼ÓČȵ½1 800 KŹ±£¬ČĖĆĒ³É¹¦ÖʵĆŌ×Ó¾§Ģåøɱł£¬Ęä½į¹¹ŗĶŠŌÖŹÓėSiO2Ō×Ó¾§ĢåĻąĖĘ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
A£®Ō×Ó¾§ĢåøɱłŅ×Ęų»Æ£¬æÉÓĆ×÷ÖĘĄä¼Į
B£®Ō×Ó¾§ĢåøɱłÓŠŗÜøßµÄČŪµćŗĶ·Šµć
C£®Ō×Ó¾§ĢåøɱłµÄÓ²¶ČŠ”£¬²»ÄÜÓĆ×÷ÄĶÄ„²ÄĮĻ
D£®1 molŌ×Ó¾§ĢåøɱłÖŠŗ¬2 mol C”ŖC¼üŗĶ2 mol C”ŖO¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
1919Äź£¬LangmuirĢį³öµČµē×ÓĢåµÄøÅÄī£¬ÓɶĢÖÜĘŚŌŖĖŲ×é³ÉµÄĮ£×Ó£¬Ö»ŅŖĘäŌ×ÓŹżĻąĶ¬£¬ø÷Ō×Ó×īĶā²ćµē×ÓŹżÖ®ŗĶĻąĶ¬£¬Ņ²æÉ»„³ĘĪŖµČµē×ÓĢ唣µČµē×ÓĢåµÄ½į¹¹ĻąĖĘ”¢ĪļĄķŠŌÖŹĻą½ü”£øł¾ŻÉĻŹöŌĄķ£¬ĻĀĮŠø÷¶ŌĮ£×ÓÖŠ£¬æռ乹ŠĶĻąĖʵďĒ(””””)
A£®SO2ŗĶO3 B£®CO2ŗĶNO2
C£®CS2ŗĶNO2 D£®PCl3ŗĶBF3
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com