
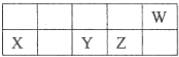
| A. | 原子半径由大到小的顺序:X、Y、Z、W | |
| B. | 元素最高正价由低到高的顺序:X、Y、Z、W | |
| C. | 简单氢化物的热稳定性由弱到强的顺序:Y、Z、W | |
| D. | 最高价氧化物的水化物的酸性由弱到强的顺序:X、Y、Z |
分析 X、Y、Z、W均为短周期元素,由位置关系可知,W处于第二周期,X、Y、Z处于第三周期,设X原子最外层电子数为a,则Y、Z、W最外层电子数依次为a+2、a+3、a+4,四种元素的原子最外层电子数之和为21,则:a+a+2+a+3+a+4=21,解得a=3,故X为Al、Y为P、Z为S、W为F.
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大;
B.F元素没有最高价正化合价+7;
C.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性越强,对应氢化物越稳定;
D.非金属性越强,最高价含氧酸的酸性越强.
解答 解:X、Y、Z、W均为短周期元素,由位置关系可知,W处于第二周期,X、Y、Z处于第三周期,设X原子最外层电子数为a,则Y、Z、W最外层电子数依次为a+2、a+3、a+4,四种元素的原子最外层电子数之和为21,则:a+a+2+a+3+a+4=21,解得a=3,故X为Al、Y为P、Z为S、W为F.
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:X>Y>Z>W,故A正确;
B.F元素没有最高价正化合价+7,故B错误;
C.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故非金属性Y<Z<W,非金属性越强,对应氢化物越稳定,故C正确;
D.同周期自左而右非金属性增强,故非金属性X<Y<Z,非金属性越强,最高价含氧酸的酸性越强,故D正确,
故选:B.
点评 本题考查元素周期表与元素周期律,侧重对元素周期律的考查,注意对元素周期律的理解掌握,难度不大.


科目:高中化学 来源: 题型:选择题
 LED产品的使用为城市增添色彩.如图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )
LED产品的使用为城市增添色彩.如图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )| A. | 该装置将化学能最终转化为电能 | |
| B. | a处通入O2 | |
| C. | b处为电池正极,发生还原反应 | |
| D. | 通入O2的电极上发生的电极反应为O2+4H++4e-=2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
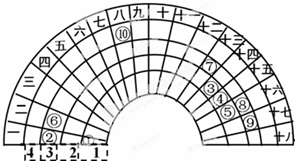 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法不正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法不正确的是( )| A. | ⑥、⑧、⑨对应原子的半径依次减小 | |
| B. | ②、⑦的最高价氧化物对应的水化物能相互反应 | |
| C. | 元素⑩处于常见周期表第四周期第VIIIB族 | |
| D. | ①分别与③、④、⑤形成的气态化合物稳定性大小为:⑤>④>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | A | B | C | D |
| 物质类型 | 离子化合物 | 共价键直接构成的物质 | 共价分子 | 稀有气体 |
| 代表物质 | NaCl | 金刚石 | 干冰 | Ne |
| 组成晶体的结构微粒 | Na+、Cl- | C | CO2 | Ne |
| 结构微粒间相互作用 | 离子键 | 共价键 | 分子间作用力 | 共价键 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应热就是反应中放出的能 | |
| B. | 在101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 | |
| C. | 由C(s,石墨)=C(s,金刚石),△H=1.9 kJ•mol-1可知,金刚石比石墨稳定 | |
| D. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{16n}{3m-2n}$ | B. | $\frac{32n}{n-m}$ | C. | $\frac{32m}{3n-2m}$ | D. | $\frac{32n}{3n-2m}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/mn | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
| A. | 元素④气态氢化物的稳定性大于元素⑤气态氢化物的稳定性 | |
| B. | 元素②气态氢化物的沸点小于元素⑤气态氢化物的沸点 | |
| C. | 元素②⑥形成的化合物具有两性 | |
| D. | 元素④的最高价氧化物的水化物比元素⑤的最高价氧化物的水化物酸性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将浓硝酸保存在无色玻璃瓶中 | |
| B. | 金属钠和钾保存在煤油中 | |
| C. | Na2CO3可以保存在玻璃塞的玻璃瓶中 | |
| D. | NaOH固体放在滤纸上称量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com