
| A. | ①③ | B. | ②④ | C. | ①② | D. | ①③④ |
分析 ①某一原子的相对原子质量是指:以一个碳-12原子质量的$\frac{1}{12}$作为标准,该原子的质量跟一个碳-12原子质量的$\frac{1}{12}$的比值;
②已知质量求物质的量,运用公式n=$\frac{m}{M}$求;
③摩尔质量是单位物质的量的物质的质量,单位为g/mol;
④氯原子的电子数为17,1个氯原子所含的电子数是17个.
解答 解:①某一原子的相对原子质量是指:以一个碳-12原子质量的$\frac{1}{12}$作为标准,该原子的质量跟一个碳-12原子质量的1/12的比值.故该氯原子的相对原子质量为$\frac{b}{\frac{a}{12}}$=$\frac{12b}{a}$,故①错误;
②根据公式n=$\frac{m}{M}$,一个该氯原子的质量是b,则1mol该氯原子的质量(摩尔质量)为(bNA)g/mol,那么mg该氯原子的物质的量即为$\frac{m}{b{N}_{A}}$mol,故②正确;
③一个该氯原子的质量是b,1mol该氯原子的质量(摩尔质量)为(bNA)g/mol,摩尔质量是单位物质的量的物质的质量,单位为g/mol,故③错误;
④一个该氯原子的质量是bg,bg该氯原子个数$\frac{bg}{b{N}_{A}g/mol}$×NA=1,1个氯原子所含的电子数是17个,bg该氯原子所含的电子数为17,故④错误.
故选D.
点评 本题考查了相对原子质量、物质的量、摩尔质量等概念,该题概念辨析要求高,平时学习是需理解这些概念与相关概念的区别和联系,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
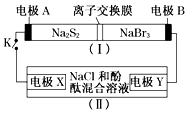 如图所示,装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图;装置(Ⅰ)的离子交换膜只允许Na+通过.电池充、放电的化学方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr.当闭合K时,X极附近溶液先变红色.下列说法正确的是( )
如图所示,装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图;装置(Ⅰ)的离子交换膜只允许Na+通过.电池充、放电的化学方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr.当闭合K时,X极附近溶液先变红色.下列说法正确的是( )| A. | 装置(Ⅰ)中Na+从左到右通过离子交换膜 | |
| B. | A电极的电极反应式为NaBr3+2Na++2e-═3NaBr | |
| C. | X电极的电极反应式为2Cl--2e-═Cl2↑ | |
| D. | 每有0.1 mol Na+通过离子交换膜,X电极上就析出标准状况下的气体1.12 L |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgSO4溶液与Ba(OH)2溶液反应:SO42-+Ba2+═BaSO4↓ | |
| B. | 向澄清的石灰水中加入过量NaHCO3溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 向Al2(SO4)3溶液中加入过量氨水溶液:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 向Ca(ClO)2溶液中通入SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量的NaHCO3逐滴加入Ba(OH)2溶液中:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| B. | NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| C. | 苯酚钠溶液中通入少量的CO2:2C6H5O-+CO2+H2O→CO32-+2C6H5OH | |
| D. | 向100 mL 3mol•L-1FeBr2溶液中通入标准状况下 3.36 LCl2:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙与盐酸反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 在CuSO4溶液中加入Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ | |
| C. | 氯气通入NaOH溶液中:Cl2+OH-═Cl-+ClO-+H2O | |
| D. | 氧化钠投入水中:O2-+H2O-═2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 两种互不相溶的液体,如汽油和水,可通过分液方法分离 | |
| B. | 因为碘易溶于酒精,所以常用酒精萃取碘水中的碘 | |
| C. | 观察钾元素焰色反应的操作:先将铂丝放在稀硫酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的外焰上进行灼烧,透过蓝色钴玻璃进行观察 | |
| D. | 将饱和FeCl3溶液滴入沸水中可得Fe(OH)3胶体,区别溶液和胶体的方法是丁达尔效应 | |
| E. | 分液时,先打开分液漏斗活塞,放出下层液体,再关闭活塞,从漏斗上口倒出上层液体 | |
| F. | 向新制的FeSO4溶液中滴入适量的NaOH溶液,放置片刻,整个反应过程的颜色变化是:浅绿色溶液→白色沉淀→灰绿色沉淀→红褐色沉淀 | |
| G. | 为除粗盐中的可溶性杂质,先加氯化钡后加碳酸钠,最后加盐酸后过滤 | |
| H. | 在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com