
 已知某市售“84消毒液”瓶体部分标签如下图所示,该“84 消毒液”通常稀释100 倍(体积之比)后使用. 请回答下列问题:
已知某市售“84消毒液”瓶体部分标签如下图所示,该“84 消毒液”通常稀释100 倍(体积之比)后使用. 请回答下列问题:
分析 (1)依据C=$\frac{1000ρω}{M}$计算溶液的物质的量浓度;
(2)A.依据配制步骤选择需要仪器;
B.定容时,还需要加入蒸馏水;
C.未用蒸馏水洗涤烧杯和玻璃棒导致溶质的物质的量偏小,依据C=$\frac{n}{V}$判断误差;
D.依据m=CVM计算需要溶质的质量;
(3)①依据C=$\frac{1000ρω}{M}$计算浓硫酸物质的量浓度,依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸体积;
②根据该物理量是否有溶液的体积有关判断;
③分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)该“84 消毒液”的物质的量浓度C=$\frac{1000×1.2×25%}{74.5}$=4.0mol/L;
故答案为:4.0;
(2)A.配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、移液、洗涤、定容、摇匀,用到的仪器:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以用不到的仪器:AB,还缺少的仪器:玻璃棒、胶头滴管,故A错误;
B.容量瓶用蒸馏水洗净后,对溶质的物质的量和溶液体积都不产生影响,且定容时需要加入蒸馏水,所以容量瓶使用前不需要烘干,故B错误;
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液浓度偏低,故C正确;
D.配制480mL,4.0mol/L次氯酸钠溶液,应选择500mL容量瓶,需要溶质的质量m=4.0mol/L×0.5L×74.5g/mol=149.0g,故D错误;
(3)①浓硫酸物质的量浓度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L,设需要浓硫酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:V×18.4mol/L=500×2.3mol/L,解得V=62.5mL;
故答案为:62.5;
②A.溶液中硫酸的物质的量n=CV,所以与溶液的体积有关,故A不选;
B.溶液具有均一性,浓度与溶液的体积无关,故B选;
C.溶质的质量与溶质的物质的量有关,依据A可知溶质的质量与溶液体积有关,故C不选;
D.溶液的密度为溶液的性质,与溶液的体积无关,故D选;
故选BD;
③A.未经冷却趁热将溶液注入容量瓶中,冷却后溶液体积偏小,溶液浓度偏高,故A选;
B.摇匀后发现液面低于刻度线,再加水至刻度线,导致溶液体积偏大,溶液浓度偏低,故B不选;
C.容量瓶中原有少量蒸馏水,对溶液体积和溶质的物质的量都不会产生影响,溶液浓度不变,故C不选;
D.定容时俯视观察液面,导致溶液体积偏小,溶液浓度偏高,故D选;
故选:BD.
点评 本题考查物质的量浓度的有关计算以及一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,题目难度不大.


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:选择题
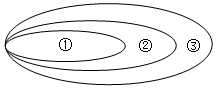
| A. | ①CO、②酸性氧化物、③氧化物 | B. | ①Na2CO3、②钠盐、③碳酸盐 | ||
| C. | ①胶体、②分散系、③混合物 | D. | ①单质、②化合物、③纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
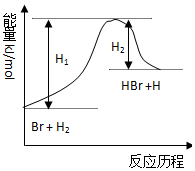
| A. | 正反应为放热反应 | |
| B. | 加入催化剂,该化学反应的反应热不改变 | |
| C. | 逆反应为吸热反应 | |
| D. | 加入催化剂可增大正反应速率,降低逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+Mg2+ CO32-Cl- | B. | Fe3+Cl- Na+H+ | ||
| C. | H+ Ag+ NO3- NH4+ | D. | CO32-H+Na+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com