
分析 (1)保持温度和压强不变,充入惰性气体,容器容积增大,等效为压强减小,平衡逆向移动;
(2)保持温度和体积不变,加入惰性气体,各组分浓度不变,平衡不移动;
(3)保持温度和压强不变,A、B、C的物质的量之比为1:2:2时,处于平衡状态.
A.物质的量均减半,A、B、C的浓度之比与原平衡相同均1:2:2,平衡不移动;
B.物质的量均加倍 A、B、C的浓度之比与原平衡相同均1:2:2,平衡不移动;
C.A、B和C的物质的量分别为2.5mol、5mol、和5mol时处于平衡状态,均增加1mol等效为前者平衡的基础上增大0.5molA;
D.A、B和C的物质的量分别为1.5mol、3mol、和3mol时处于平衡状态,均进行1mol等效为前者平衡的基础上移走0.5molA.
解答 解:(1)保持温度和压强不变,充入惰性气体,容器容积增大,等效为压强减小,平衡逆向向移动,C的物质的量减小,故答案为:减小;
(2)保持温度和体积不变,加入惰性气体,各组分浓度不变,平衡不移动,A的转化率不变,故答案为:不变;
(3)保持温度和压强不变,A、B、C的物质的量之比为1:2:2时,处于平衡状态;
A.物质的量均减半,A、B、C的浓度之比与原平衡相同均1:2:2,恒温恒压下为等效平衡,平衡不移动,故A不符合;
B.物质的量均加倍 A、B、C的浓度之比与原平衡相同均1:2:2,恒温恒压下为等效平衡,平衡不移动,故B不符合;
C.A、B和C的物质的量分别为2.5mol、5mol、和5mol时处于平衡状态,均增加1mol等效为前者平衡的基础上增大0.5molA,平衡正向移动,故C符合;
D.A、B和C的物质的量分别为1.5mol、3mol、和3mol时处于平衡状态,均进行1mol等效为前者平衡的基础上移走0.5molA,平衡逆向移动,故D不符合,
故选:C.
点评 本题考查化学平衡移动、等效平衡,难度中等,关键是理解效平衡规律:1、恒温恒容,反应前后气体体积不等,按化学计量数转化一边,对应物质满足等量;反应前后气体体积相等,按化学计量数转化一边,对应物质满足等比,2:恒温恒压,按化学计量数转化一边,对应物质满足等比.


科目:高中化学 来源: 题型:选择题
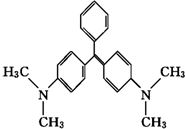 孔雀石绿是化工产品,具有较高毒性,高残留,容易致癌、致畸.其结构简式如图所示.下列关于孔雀石绿的说法正确的是( )
孔雀石绿是化工产品,具有较高毒性,高残留,容易致癌、致畸.其结构简式如图所示.下列关于孔雀石绿的说法正确的是( )| A. | 孔雀石绿的分子式为C23H25N2 | |
| B. | 1 mol孔雀石绿在一定条件下最多可与6 mol H2发生加成反应 | |
| C. | 孔雀石绿属于芳香族化合物 | |
| D. | 孔雀石绿苯环上的一氯取代物有6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 分子式 | C3H8O | C4H8Cl2 | C7H16 | C8H10 |
| 限定条件 | 能使KMnO4溶液褪色 | 分子中含有2个甲基 | 分子中含有3个甲基 | 芳香烃、能得到三种一硝基化物 |
| 数目 | 2 | 3 | 2 | 3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “忽闻海上有仙山,山在虚无缥缈间”的海市蜃楼是一种自然现象,与胶体知识有关 | |
| B. | “水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化 | |
| C. | “滴水石穿、绳锯木断”不包含化学变化 | |
| D. | “落汤螃蟹着红袍”肯定发生了化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化合物 | Na2CO3 | NaHCO3 | NaCl |
| 质量(kg) | 814.8 | 400.3 | 97.3 |
| 化合物 | Na2CO3 | NaHCO3 | NaCl |
| 质量(kg) | 137.7 | 428.8 | 97.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 3:2 | B. | 4:3 | C. | 4:1 | D. | 2:l |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com