
| A. | 该反应是一个放热反应 | |
| B. | 参加反应的氢气和氧气的总能量高于反应生成的水的总能量 | |
| C. | 在该化学反应中,破坏旧化学键吸收的能量大于形成新化学键释放的能量 | |
| D. | 发生反应时,断开反应物中的H-H键和O-O键都要吸收能量 |
分析 A、氢气在氧气中燃烧是放热反应;
B、反应物总能量高于生成物,反应放热;
C、破坏旧化学键吸收的能量小于形成新化学键释放的能量,反应放热;
D、反应中断裂化学键吸收的能量.
解答 解:A、氢气在氧气中点燃发生燃烧,是放热反应,故A正确;
B、反应是放热反应,依据反应前后能量守恒得到,反应物总能量高于生成物,故B正确;
C、反应是放热反应,破坏旧化学键吸收的能量小于形成新化学键释放的能量,故C错误;
D、反应中断裂化学键吸收的能量,所以断开反应物中的H-H键和O-O键都要吸收能量,故D正确;
故选C.
点评 本题考查了化学反应能量变化分析,主要是能量守恒和反应实质的理解应用,题目较简单.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:实验题
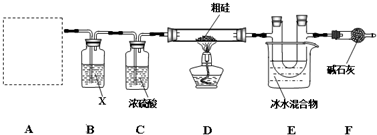
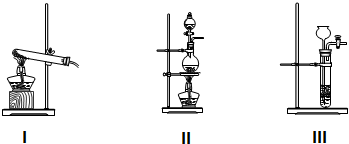
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减小容器体积,平衡向右移动 | |
| B. | 加入催化剂,平衡不移动故正逆反应速率不变 | |
| C. | 增大c(X),X的转化率增大 | |
| D. | 降低温度,Y的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O的摩尔质量是18g | B. | 1mol氧的质量是16g | ||
| C. | 氧气的摩尔质量是32g•mol-1 | D. | 2molH2的摩尔质量是4g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
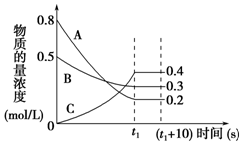
| A. | t1s时反应物A的转化率为60% | |
| B. | 在t1~(t1+10)s时,v(A)=v(B)=0 | |
| C. | 该反应的化学方程式为3A+B?2C | |
| D. | 0~t1s内A的反应速率为v(A)=$\frac{0.2}{{t}_{1}}$mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴离子具有氧化性 | B. | 氯气是还原剂 | ||
| C. | 氯气发生氧化反应 | D. | 氧化性:Cl2>Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
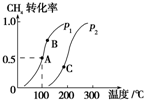 利用天然气可制得以H2、CO等为主要组成的工业原料合成气,反应为:CH4(g)+H2O(g)?CO(g)+3H2(g).
利用天然气可制得以H2、CO等为主要组成的工业原料合成气,反应为:CH4(g)+H2O(g)?CO(g)+3H2(g).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com