
分析 先根据该焊锡中锡和铅的质量分数计算出二者质量,然后根据n=$\frac{m}{M}$分别计算出该焊锡中含有锡和铅的物质的量.
解答 解:铅的摩尔质量为207g/mol,锡的摩尔质量为119g/mol,
100克某种焊锡中含锡43.2%及含铅56.8%,则该焊锡中含有锡的物质的量为:$\frac{100g×43.2%}{119g/mol}$≈0.363mol,含有铅的物质的量为:$\frac{100g×56.8%}{207g/mol}$≈0.274mol,
故答案为:0.363mol;0.274mol.
点评 本题考查了物质的量的计算,题目难度不大,明确质量分数的含义为解答关键,注意掌握物质的量与摩尔质量之间的关系,试题培养了学生的化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属Na着火,可立即用水扑灭 | |
| B. | 炒菜时油锅里着火了,可关掉火源并用锅盖盖灭 | |
| C. | 贮氯罐意外泄漏,应向贮氯罐周围空中喷洒稀NaOH溶液 | |
| D. | 闻氯气的气味时,应用手在瓶口轻轻煽动,使少量氯气进入鼻孔 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
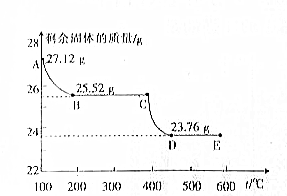
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 序号 | 0.01mol/L KIO3酸性溶液 (含淀粉)的体积/mL | 0.01mol/L Na2SO3溶 液的体积/mL | 水的体 积/mL | 实验温 度/℃ | 出现蓝色 的时间/s |
| ① | 5 | 5 | V1 | 0 | |
| ② | 5 | 5 | 40 | 25 | |
| ③ | 5 | V2 | 35 | 25 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①③ | C. | ②④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+的电子排布图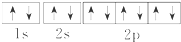 | |
| B. | Na+的结构示意图: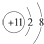 | |
| C. | 基态Na原子的电子排布式:1s22s22p53s2 | |
| D. | 基态Na原子的价电子排布式:3s1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com