
| 10-7×0.01 | ||
|
| 2×10-9 |
| (c-0.02) |
| 2×10-9 |
| (c-0.02) |


科目:高中化学 来源: 题型:
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
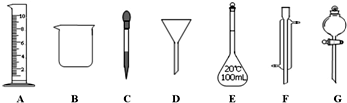
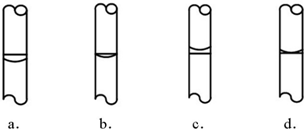
查看答案和解析>>
科目:高中化学 来源: 题型:
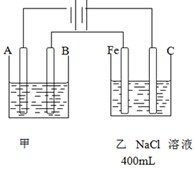 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
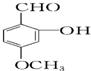 b.
b.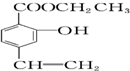 c.
c.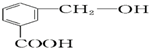
查看答案和解析>>
科目:高中化学 来源: 题型:
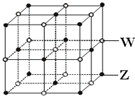 X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素,已知:
X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素,已知:| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com