
| CaS04 | Mg2(OH)2C03 | CaC03 | BaS04 | BaC03 |
| 2.6×1 0-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×1 0-3 |
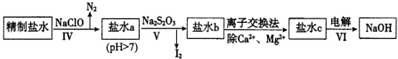
分析 (1)①根据检验铁离子的方法进行分析Fe3+是否除尽的方法;
②根据表中数据分析BaSO4与CaSO4的溶解度大小,溶解度越小,沉淀越完全;
③镁离子能够与碳酸根离子反应生成Mg2(OH)2CO3沉淀,从而除去镁离子杂质,据此写出反应的离子方程式;
④根据BaCO3、CaCO3、Mg2(OH)2CO3 的溶解度进行分析;
(2)①次氯酸根离子具有强氧化性,能够氧化铵根离子和碘离子;
②Na2S2O3具有还原性,能够与碘酸根离子发生氧化还原反应,同时被氧化成硫酸根离子,据此写出反应的离子方程式;
③根据电解原理及水的电离平衡H2O?H++OH-进行分析在电解槽的阴极区生成NaOH原理.
解答 解:(1)①检测Fe3+是否除尽的方法为:取少量过程II后的滤液于试管中,滴加几滴KSCN 溶液,若溶液不变红,说明Fe3+已除尽,反之没除尽,
故答案为:取少量过程II后的滤液于试管中,滴加几滴KSCN 溶液,若溶液不变红,说明Fe3+已除尽,反之没除尽;
②硫酸钡的溶度积为2.4×10-4,硫酸钙的溶度积为2.6×10-2,显然硫酸钙的溶度积大于硫酸钡,即BaSO4的溶解度比CaSO4的小,可将SO42-沉淀更完,
故答案为:BaSO4的溶解度比CaSO4的小,可将SO42-沉淀更完;
③镁离子能够与碳酸根离子反应生成难溶物Mg2(OH)2CO3,反应的离子方程式为:2Mg2++2CO32-+H2O═Mg2(OH)2CO3↓+CO2↑,
故答案为:2Mg2++2CO32-+H2O═Mg2(OH)2CO3↓+CO2↑;
④根据步骤数据可知,在BaCO3、CaCO3、Mg2(OH)2CO3 中,BaCO3的溶解度最大,若Ba2+沉淀完全,则说明Mg2+ 和Ca2+也沉淀完全,
故答案为:Ba2+;
(2)①过程Ⅳ加入次氯酸钠,次氯酸根离子能够氧化NH4+、I-,从而除去杂质NH4+、I-,
故答案为:NH4+、I-;
②盐水b中含有SO42-,Na2S2O3将IO3-还原为I2,Na2S2O3被氧化成硫酸根离子,反应的离子方程式为:5S2O32-+8IO3-+2OH-═4I2+10SO42-+H2O,
故答案为:5S2O32-+8IO3-+2OH-═4I2+10SO42-+H2O;
③电解过程中,H+在阴极上得电子变成H2逸出,使H2O?H++OH-电离平衡向右移动,OH-在阴极区浓度增大,Na+向阴极区移动,最后NaOH在阴极区生成,
故答案为:H+在阴极上得电子变成H2逸出,使H2O?H++OH-电离平衡向右移动,OH-在阴极区浓度增大,Na+向阴极区移动,最后NaOH在阴极区生成.
点评 本题考查了粗盐的提纯、难溶电解质的沉淀平衡及转化、电解原理、离子方程式的书写等知识,题目难度中等,试题涉及的题量较大,知识点较多,注意掌握粗盐的提纯方法、物质的分离与提纯原则,明确电解原理及应用方法,能够正确书写离子方程式.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:选择题
| A. | H2SO4溶液 | B. | AgNO3溶液 | C. | NaOH溶液 | D. | 氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1-丙醇与浓氢溴酸反应:CH3CH2 CH2OH+HBr$\stackrel{△}{→}$CH3CH2 CH2Br+H2O | |
| B. | 1-溴丙烷与氢氧化钠溶液共热:CH3CH2 CH2Br+NaOH$→_{△}^{水}$CH3CH2 CH2OH+NaBr | |
| C. | 苯酚钠中通入少量二氧化碳:2 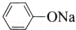 +CO2+H2O→2 +CO2+H2O→2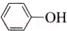 +Na2CO3 +Na2CO3 | |
| D. | 蔗糖在稀硫酸作用下水解:C12H22O11(蔗糖)+H2O$→_{△}^{稀硫酸}$C6H12O6(果糖)+C6H12O6(葡萄糖) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液中滴入AgNO3溶液,产生白色沉淀,该溶液中一定含Cl- | |
| B. | 某溶液与淀粉碘化钾溶液反应后显蓝色,证明溶液是氯水或溴水 | |
| C. | 将氟气通入氯化钠水溶液中,一定有氢氟酸和O2生成 | |
| D. | 实验证明氯水也能导电,所以氯水是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20:1 | B. | 1:20 | C. | 10:1 | D. | 1:10 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A钻木取火 | B电暖扇取暖 | C酒精灯燃烧 | D燃煤发电 |
| 图片 |  |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
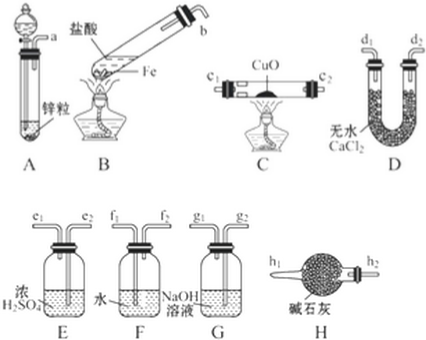
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com