
下列关于铁及其化合物的有关说法正确的是( )
A.赤铁矿的主要成分是Fe3O4
B.铁与水蒸气在高温下的反应产物为Fe2O3和H2
C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
D.Fe3+与KSCN溶液反应产生红色沉淀
科目:高中化学 来源:2014高考化学苏教版总复习 专题7化学反应速率与化学平衡练习卷(解析版) 题型:选择题
将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应:H2NCOONH4(s)  2NH3(g)+CO2(g),在不同温度下,该反应平衡状态时的部分数据见下表。下列说法正确的是( )
2NH3(g)+CO2(g),在不同温度下,该反应平衡状态时的部分数据见下表。下列说法正确的是( )
温度 | 平衡浓度/(mol·L-1) | |
c(NH3) | c(CO2) | |
T1 | 0.1 |
|
T2 |
| 0.1 |
A.若T2>T1,则该反应的ΔH<0
B.向容器中充入N2,H2NCOONH4质量增加
C.NH3体积分数不变时,说明该反应达到平衡
D.T1、T2时,H2NCOONH4转化的Δn(T2)=2Δn(T1)
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题5微观结构与物质的多样性练习卷(解析版) 题型:选择题
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
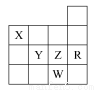
A.常压下五种元素的单质中W单质的沸点最高
B.Z元素的最高价氧化物对应的水化物酸性最强
C.X的氢化物比同族元素的氢化物沸点低
D.Y、Z和W的阴离子半径依次增大
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题3从矿物到基础材料练习卷(解析版) 题型:填空题
日常生活中使用的铝合金中的铝来自于电解氧化铝。工业上电解氧化铝要求其纯度不得低于98.2%,而天然铝土矿的氧化铝含量为50%~70%,杂质主要为SiO2、Fe2O3、CaO、MgO、Na2O等。工业生产铝锭的工艺流程示意图如下:
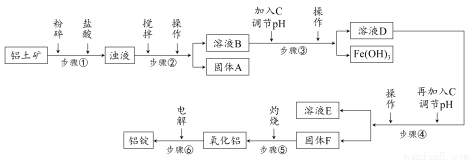
一些氢氧化物沉淀的pH如下表:
沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 |
开始沉淀pH(离子初始浓度0.01 mol/L) | 4 | 2.3 | 10.4 |
完全沉淀pH(离子浓度<10-5 mol/L) | 5.2 | 4.1 | 12.4 |
请回答下列问题:
(1)加入盐酸时,氧化铝发生反应的离子方程式为________________。
(2)实验室进行步骤②③④的操作名称为________。
(3)固体A的化学式为________,物质C的化学式为________;溶液中的Na+、Ca2+、Mg2+是在步骤________中分离出去的。
(4)步骤③调节pH的数值范围为________,步骤④调节pH的数值范围为________。
(5)步骤⑥反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题3从矿物到基础材料练习卷(解析版) 题型:选择题
下列各组物质中,不是按下图所示(“→”表示一步完成)关系相互转化的是( )
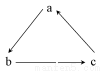
选项abc
AFeFeCl3FeCl2
BCl2NaClONaCl
CSiSiO2H2SiO3
DHNO3NONO2
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题3从矿物到基础材料练习卷(解析版) 题型:选择题
新型镁合金被大量应用于制笔记本电脑的外壳、竞赛自行车的框架等,这些实际应用充分体现了镁合金的下列哪些优异性能( )
①熔点低;②硬度大;③延展性好;④导电性强;⑤密度小;⑥耐腐蚀
A.①②③ B.②③④ C.①③⑥ D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题2从海水中获得的化学物质练习卷(解析版) 题型:选择题
把一块镁铝合金投入到1 mol/L盐酸里,待合金完全溶解后,往溶液里加入1 mol/L NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图A所示。下列说法中不正确的是( )
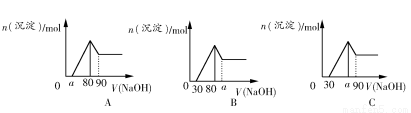
A.a的取值范围为0≤a<50
B.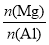 的最大值为2.5
的最大值为2.5
C.若将关系图改为图B,则a的取值范围为80<a<90
D.若将关系图改为图C,则a的取值范围为75<a<90
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题1化学家眼中的物质世界练习卷(解析版) 题型:填空题
由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、NH、Ba2+、Al3+、Fe3+、Cl-、SO42-、CO32-,将该混合物溶于水后得澄清溶液,现取3份100 mL该溶液分别进行如下实验:
序号 | 实验内容 | 实验结果 |
1 | 加过量盐酸 | 无气体产生 |
2 | 加足量NaOH溶液并加热 | 收集到气体1.12 L(已折算成标准状况下的体积),并有红褐色沉淀生成,将沉淀过滤洗涤、干燥、灼烧,称重得1.60 g固体。 |
3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量 | 第一次称量读数为2.33 g |
试回答下列问题:
(1)根据实验1对CO32-是否存在的判断是________,(填“一定存在”“一定不存在”或“不能确定”);根据实验1~3判断混合物中一定不存在的离子是________。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
阴离子符号 | 物质的量浓度(mol·L-1) |
|
|
|
|
|
|
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题12物质结构与性质练习卷(解析版) 题型:填空题
有E、Q、T、X、Z五种前四周期元素,原子序数E<Q<T<X<Z。E、Q、T三种元素的基态原子具有相同的能层和能级,且I1(E)<I1(T)<I1(Q),其中基态Q原子的2p轨道处于半充满状态,且QT2+与ET2互为等电子体。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
(1)写出QT2+时的电子式:________,基态Z原子的核外电子排布式为________。
(2)Q的简单氢化物极易溶于T的简单氢化物,其主要原因有________等两种。
(3)化合物甲由T、X两元素组成,其晶胞如图1所示,甲的化学式为____。
(4)化合物乙的晶胞如图2所示,乙由E、Q两元素组成,硬度超过金刚石。
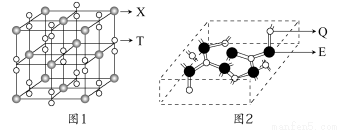
①乙的晶体类型为________,其硬度超过金刚石的原因是________。
②乙的晶体中E、Q两种元素原子的杂化方式均为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com