
| A.配制FeCl3(aq):称取一定质量的FeCl3(s),加水溶解,再加入稀盐酸酸化 |
| B.钠与水的反应:取绿豆大小的金属钠放入烧杯,再滴入两滴酚酞试液,最后加入水 |
| C.析出溶质晶体:接近饱和的热溶液,冷却速度越慢得到的晶体颗粒越大 |
| D.实验室制氢气:为了加快反应速率,向稀H2SO4中滴加少量Cu(NO3)2(aq) |
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | 向AgI沉淀中滴入饱和KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | 向某溶液加入CCl4 | 液体分层,下层CCl4显紫色 | 原溶液中存在I- |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 分别测定0.1mol/LNa2CO3和苯酚钠溶液的pH | 前者pH比后者的大 | 酸性:苯酚>碳酸 |
| B | 向无色溶液A中加入稀硫酸 | 产生淡黄色沉淀和无色气体 | A中含S2O32-离子 |
| C | CuSO4和H2SO4混合溶液中加入Zn | 锌表面附着红色物质;产生无色气体 | 氧化性:Cu2+>H+ |
| D | 向0.01mol/L的KCl、KI混合液中滴加AgNO3溶液 | 先出现黄色沉淀 | 溶解出Ag+的能力:AgCl > AgI |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
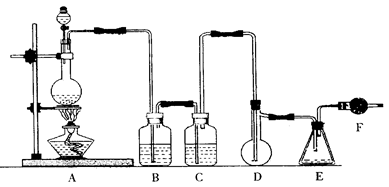
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验步骤 | 预期现象和结论 |
 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 | |
| 步骤2:取适量滤液于试管中,滴加稀硫酸。 | |
| 步骤3:取适量步骤1中的沉淀于试管中,_____。 | |
| 步骤4: | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

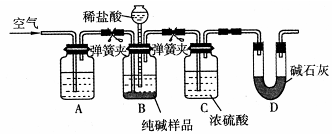
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.食盐水放在试管中进行蒸发可得到NaCl固体 |
| B.滴定管在加入反应液之前一定要用所要盛装的反应液润洗2—3遍 |
| C.分液漏斗可用于任何液体混合物的分离和组装滴加液体制气体的发生装置 |
| D.可用量筒快速配制一定体积、一定物质的量浓度的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com