
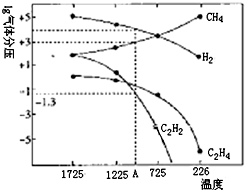
 乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产.
乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产.| 3 |
| 2 |
| 3 |
| 2 |
| Xmol/L |
| 2 |
| Xmol |
| 2 |
| X |
| 2 |
| 0.2mol/L |
| 0.3mol/L |
| P(C2H2)?P3(H2) |
| P2(CH4) |
| 0.05×(104)3 |
| (103)2 |


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
| A、Fe3+、NO3-、Cl-、Na+ |
| B、Ca2+、HCO3-、Cl-、K+ |
| C、NH4+、Fe2+、SO42-、NO3- |
| D、Cl-、SO42-、K+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,16 g CH4中含有的原子总数为5NA |
| B、标准状况下,11.2 LCH3OH中含有的共价键数目为2.5NA |
| C、常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
| D、标准状况下,0.1 mol Cl2被氢氧化钠溶液完全吸收,转移的电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
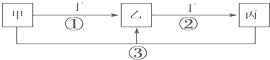 已知甲、乙、丙、丁是中学化学的常见物质,且甲、乙、丙均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).
已知甲、乙、丙、丁是中学化学的常见物质,且甲、乙、丙均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).查看答案和解析>>
科目:高中化学 来源: 题型:
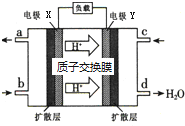 绿色电源“二甲醚-氧气燃料电池”的工作原理如图,
绿色电源“二甲醚-氧气燃料电池”的工作原理如图,查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2是一种酸性氧化物 |
| B、碳氧两种元素只能组成CO2 |
| C、干冰的主要成份是CO2 |
| D、固态CO2的密度比气态CO2的密度大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol任何气体的体积都是22.4 L |
| B、2 mol氯化钠固体溶解于1 L水所得盐酸物质的量为2 mol/L |
| C、含有NA个氦原子的氦气在标准状况下的体积约为11.2 L |
| D、32 g O2中含有氧原子数为1.204×1024 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com