
| A. | 由于电流的作用,酸、碱、盐溶于水发生电离 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm | |
| C. | 存在自由移动的离子是电解质溶液导电的原因 | |
| D. | 醋酸溶液中存在H+、CH3COOH、CH3COO-等微粒,故醋酸是弱电解质 |
分析 A.酸碱盐在水溶液中电离时是在水分子作用下电离的;
B.胶体微粒直径在1-100nm之间;
C.含有自由移动离子或电子的物质能导电;
D.部分电离的电解质是弱电解质,完全电离的电解质是强电解质.
解答 解:A.酸碱盐在水溶液中电离时是在水分子作用下电离的,不需要外加电源,故A错误;
B.胶体微粒直径在1-100nm之间,胶体具有丁达尔效应,不能透过半透膜,故B正确;
C.含有自由移动离子或电子的物质能导电,所以含有自由移动离子的电解质溶液能导电,故C正确;
D.部分电离的电解质是弱电解质,完全电离的电解质是强电解质,根据溶液中存在的微粒知,醋酸部分电离,所以醋酸的弱电解质,故D正确;
故选A.
点评 本题考查电解质的电离、电解质强弱判断、电解质导电性原理、胶体等知识点,明确基本概念及基本原理是解本题关键,侧重考查学生分析判断能力,注意电解质与导电性的关系,易错选项是A.


科目:高中化学 来源: 题型:解答题
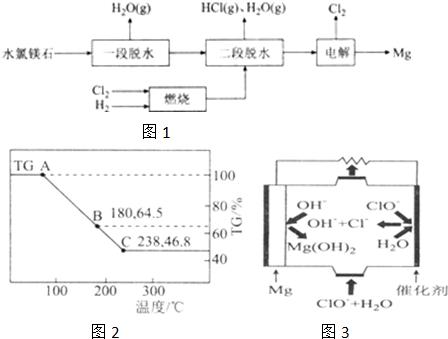
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | .碳酸氢钙溶液中加入氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| B. | 用胃舒平治疗胃酸过多:Al(OH)3+3H+═Al3++3H2O | |
| C. | Na与H2O反应:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为22.4L | |
| B. | 常温常压下,28g N2中含有的原子数为NA | |
| C. | 标准状况下22.4L Cl2与足量的水充分反应,转移的电子数为NA | |
| D. | 标准状况下,11.2LH2O含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性:Na>Mg>Al | B. | 第一电离能:Na<Mg<Al | ||
| C. | 电负性:Na>Mg>Al | D. | 碱性:NaOH<Mg(OH)2<Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
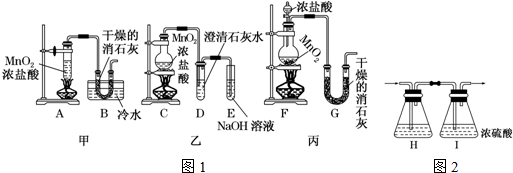
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
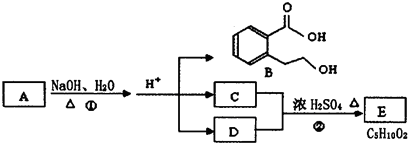
 .
. .
.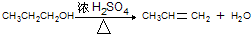 .
.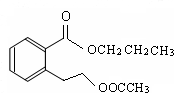 .
.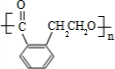 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 莫言 | B. | 屠呦呦 | C. | 侯德榜 | D. | 徐光宪 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com