
|
在周期表的前三个周期中,位置相邻的三种元素的质子数之和为33,则有关这三种元素的下列说法正确的是 | |
A. |
可能在同一周期 |
B. |
可能在同一主族 |
C. |
可能有两种元素在第二周期 |
D. |
可能有两种元素在第三周期 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
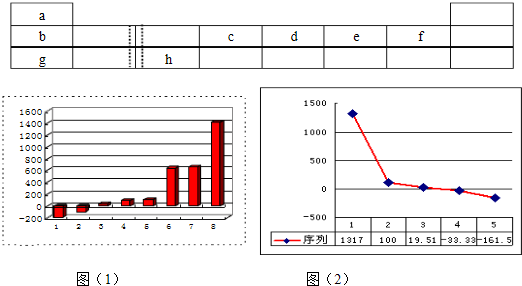





查看答案和解析>>
科目:高中化学 来源: 题型:
| a | |||||||
| b | c | d | e | f | |||
| g | h | i | |||||

查看答案和解析>>
科目:高中化学 来源:2011--2012学年四川省成都二十中高二上学期期中考试化学试卷 题型:填空题
(8分)下表由元素周期表的前三周期去掉副族上方的空白区域后组合而成,表中虚线处为ⅡA、ⅢA族的连接处,请用相应的化学用语或符号回答下列问题:
| a | | | | | | | |
| b | | | c | d | e | f | |
| g | | h | | | | | |


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com