
| A. | 降低温度可以加快反应速率 | |
| B. | 如果反应开始时加入2molN2和6molH2,则达到平衡时,n(N2):n(H2)=1:3 | |
| C. | 达到化学反应限度时,生成2mol NH3 | |
| D. | 1mol N2 和3mol H2的总能量低于2mol NH3的总能量 |
分析 A.降低温度后化学反应速率会减小;
B.氮气、氢气的初始物质的量之比为1:3,反应消耗的物质的量之比为1:3,则平衡时二者的物质的量之比仍然为1:3;
C.可逆反应的反应物不能完全转化;
D.反应放热,说明反应物能量高于生成物.
解答 解:A.降温化学反应速率应该减慢,故A错误;
B.如果反应开始时加入2molN2和6molH2,反应过程中氮气和氢气消耗的物质的量之比为1:3,则达到平衡时n(N2):n(H2)=1:3,故B正确;
C.合成氨是可逆反应,可逆反应的反应物不能完全转化为生成物,所以1mol N2和3mol H2发生反应生成的氨气少于2mol,故C错误;
D.该反应为放热反应,说明1mol N2和3mol H2的总能量高于2mol NH3的总能量,故D错误;
故选B.
点评 本题考查了化学平衡及其影响,题目难度中等,涉及可逆反应特点、化学平衡的影响因素、化学反应速率及其影响等知识,明确化学平衡及其影响因素为解答关键,试题培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 往NaOH溶液中通入过量SO2:SO2+2OH-═SO32-+H2O | |
| B. | 锌与稀硝酸反应:Zn+2H+═Zn2++H2↑ | |
| C. | 向氯化铵的溶液中加入足量浓KOH溶液并加热:NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3•H2O | |
| D. | 向氯水中通入SO2气体:Cl2+SO2+2H2O═4H++2Cl-+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(H2)=0.3 mol•L-1•min-1 | B. | v(N2)=0.05 mol•L-1•s-1 | ||
| C. | v(N2)=0.2 mol•L-1•min-1 | D. | v(NH3)=0.3 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为提高反应速率和原料利用率,硫铁矿要在“沸腾”状态下燃烧 | |
| B. | 为防止催化剂中毒,气体在进接触室前要先净化 | |
| C. | 接触室中热交换器的主要作用是预热未反应的气体和冷却反应后的气体 | |
| D. | 吸收塔中SO3从下而上,水从上而下喷,剩余气体从上部出来循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 压强Mpa 转化率% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
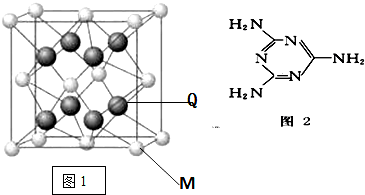
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg在CO2中燃烧生成MgO和C,是放热反应 | |
| B. | 工业上通过电解MgCl2溶液制取金属镁 | |
| C. | Mg和稀硫酸反应时,滴加少量硫酸铜溶液,能加快反应速率 | |
| D. | 镁可以用来制造信号弹和焰火,MgO可以作耐高温材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com