
分析 (1)根据生成氨气的物质的量,利用物质的量之比等于化学计量数之比计算参加反应的氮气的物质的量,t时刻时氮气的物质的量与参加反应的氮气的物质的量之和为X的值;
(2)计算出混合气体总的物质的量,利用体积分数计算氨气的物质的量.
解答 解:(1)反应进行到t时,测的N2为10mol,NH3为4mol,由方程式可知,参加反应的氮气的物质的量为4$\frac{1}{2}$mol=2mol,故氮气的起始物质的量为:10mol+2mol=12mol,即X=12.
故答案为:X的值为12;
(2)反应达平衡时,混合气体为$\frac{672L}{22.4mol/L}$=30mol,其中NH3的物质的量为30mol×20%=6mol.参加反应的氮气的物质的量为6mol×$\frac{1}{2}$=3mol,N2转化率=$\frac{3mol}{12mol}$×100%=25%;
根据三段式:N2(g)+3H2(g)?2NH3(g)
起始量:12 Y 0
转化量:3 9 6
平衡量:9 30-9-6=15 6
则Y=15+9=24mol.
故答案为:N2的转化率为25%,Y的值为24.
点评 考查化学平衡的有关计算,难度不大,注意基础知识的积累和化学平衡中三段式计算的掌握


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:选择题
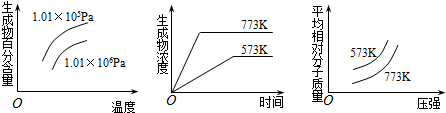
| A. | N2(g)+3H2(g)?2NH3(g) (正反应为放热反应) | |
| B. | 2SO3(g)?2SO2(g)+O2(g) (正反应为吸热反应) | |
| C. | 4NH3(g)+5O2(g)?4NO+6H2O(g) (正反应为放热反应) | |
| D. | 2HI(g)?I2(g)+H2(g) (正反应为吸热反应) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
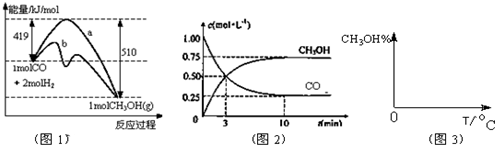
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
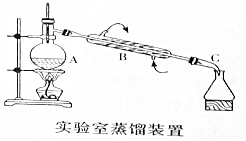 如图是用自来水制备蒸馏水的实验装置图.
如图是用自来水制备蒸馏水的实验装置图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学反应及平衡常数 | 平衡常数数值 | ||
| 500℃ | 800℃ | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | 2.5 | 0.375 |
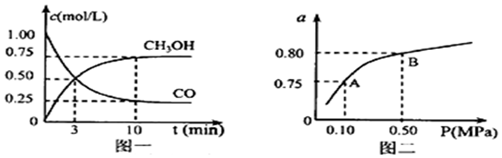
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(OH)2 溶液 | B. | 饱和NaCl溶液 | C. | 自来水 | D. | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家分获,以表彰他们在“分子马达”研究方面的成就,一种光驱分子马达结构如图所示.有关该分子的说法正确的是( )
2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家分获,以表彰他们在“分子马达”研究方面的成就,一种光驱分子马达结构如图所示.有关该分子的说法正确的是( )| A. | 该分子中有两个手性碳原子 | |
| B. | 两个苯环可以处于同一平面 | |
| C. | 能与NaHCO3和酸性KMnO4溶液反应 | |
| D. | 1mol该分子最多可与2molH2发生加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验后剩余的钠粒,需要放回原试剂瓶中 | |
| B. | 少量的钠可以保存煤油中,如果露置在空气中会迅速和氧气反应生成过氧化钠 | |
| C. | 钠长期放罝在空气中,最终将变成碳酸钠 | |
| D. | 当钠与硫酸铜溶液反应时,有大量蓝色沉淀出现 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com