
0.5 L 1 mol·L-1 FeCl3溶液与0.2 L 1 mol·L-1 KCl溶液中的Cl-的数目之比为( )。
A.5∶2 B.3∶1 C.15∶2 D.1∶3
科目:高中化学 来源: 题型:
下列反应中,属于氧化还原反应的是( )
A.2 H2O2  2 H2O + O2↑
2 H2O + O2↑
B.2 Al(OH)3  Al2O3 + 3 H2O
Al2O3 + 3 H2O
C.FeO + 2 HCl = FeCl2 + H2O
D. CuCl2 + 2 NaOH = Cu(OH)2↓+ 2NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
在1 L HNO3和H2S04的混合溶液中,两种酸的物质的量浓度之和为O.6 mol/l,向该溶液中加入足量铜粉,加热,充分反应,当HNO3与H2S04的物质的量比为x:y 时所得溶液中Cu2+物质的量浓度最大,则x:y为
A.3:8 B.2:3 C.1:4 D.1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
吸食“摇头丸”会严重破坏中枢神经,其化学式为C9H13N,请回答:
2 mol“摇头丸”所含的碳原子的物质的量为______mol,氢原子的物质的量为______mol,氮原子的物质的量为______mol,氮原子的个数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在无土栽培中,需配制1L含0.50 mol·L-1的NH4Cl、0.16 mol·L-1KCl、0.24 mol·L-1K2SO4的混合溶液,但当时没有K2SO4固体,若用(NH4)2SO4固体代替,需用KCl、NH4Cl、(NH4)2SO4三种固体的物质的量(单位为 mol)分别为( )
A.0.40、0.50、0.12 B.0.66、0.50、0.24
C.0.64、0.50、0.24 D.0.64、0.02、0.24
查看答案和解析>>
科目:高中化学 来源: 题型:
关于中和热测定的说法错误的是( )
A.实验需用到的主要玻璃仪器包括大、小烧杯,温度计,环形玻璃搅拌棒及泡沫塑料板、碎泡沫塑料(或硬纸板、碎纸条)等;
B.盐酸与某强碱中和放出的热量随反应物用量的改变而改变,但中和热不变;
C.NaOH稍过量的目的是保证盐酸完全被NaOH中和;
D.测定结果准确与否的关键是尽量减小热量损失及准确读取混合溶液的最高温度等。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列化学用语中,正确的是( )
A、电解饱和食盐水时,阳极的电极反应式为:2Cl- -2e-= Cl2 ↑
B、氢氧燃料电池的负极反应式:O2 + 2H2O + 4e- = 4OH-
C、镀件上电镀铜时,纯铜做阴极,电极反应式为:Cu -2e- = Cu2+
D、钢铁发生电化学腐蚀的正极反应式:Fe-2e- = Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
二甲醚(CH3OCH3)被称为21世纪界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)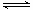 CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1
②2CH3OH(g)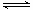 CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g)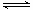 CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为 。
A.加入某物质作催化剂 B.加入一定量CO C.反应温度降低 D.增大容器体积
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率
为 ;
若反应物的起始浓度分别为:c(CO)=4 mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2 mol/L,a= mol/L。
(3)催化反应室中总反应3CO(g)+3H2(g)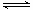 CH3OCH3(g)+CO2(g)的△H= 。
CH3OCH3(g)+CO2(g)的△H= 。
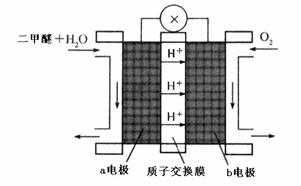
(4)“二甲醚燃料电池”是一种绿色电源,其工作原理如上图所示。b电极是 极,写出b电极上发生的电极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列依据热化学方程式得出的结论正确的是( )
A.已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ· mol-1说明2 mol H2(g)和1 mol O2(g)的能量总和小于2 mol H2O(g)的能量
B.已知C(s,石墨)===C(s,金刚石) ΔH>0,则金刚石比石墨稳定
C.已知NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,
则含20 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量
D.已知2C(s)+2O2(g)===2CO2(g) ΔH1
2C(s)+O2(g)===2CO(g) ΔH2,则ΔH1>ΔH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com