
| A. | ①②③ | B. | ②③ | C. | ①② | D. | ④⑤ |
分析 ①如果存在双键,能够使溴水褪色;
②碳碳单键键常与碳碳双键键长比相等;
③由于苯环对测链的影响,苯环上的甲基能够被高锰酸钾氧化;
④无论苯分子无单双键交替结构,间二甲苯都只有1种;
⑤苯不能与氢氧化钠反应.
解答 解:①如果苯是单双键交替结构,则苯应该能与溴水发生加成反应,苯不能因发生化学反应而使溴水溶液褪色说明不存在双键,故①正确;
②若苯是单双键交替结构,则碳碳键键长不同,而实际分子中碳碳之间的键长均相等证明苯分子无单双键交替结构?,故②正确;
③甲苯是苯的同系物,苯不能使酸性高锰酸钾溶液褪色,甲苯能够被酸性高锰酸钾氧化生成苯甲酸,故③错误;
④无论苯分子无单双键交替结构,间二甲苯都只有1种,所以间二氯苯没有同分异构体不能证明了苯分子不是单双键交替,故④错误;
⑤硝基苯中含有苯、浓硝酸、浓硫酸杂质,向其中加入氢氧化钠溶液后分液,只能出去浓硝酸、浓硫酸,不能除去苯,故⑤错误;
故选:C.
点评 本题考查了苯及其化合物,侧重考查苯的结构,明确苯环中碳碳双键的独特性是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | υ(A2)=0.4 mol•L-1•s-1 | B. | υ(B2)=0.8 mol•L-1•s-1 | ||
| C. | υ(C)=0.6 mol•L-1•s-1 | D. | υ(D)=0.6 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 被提纯物质 | 除杂试剂 | 分离方法 |
| ① | 苯甲酸(不溶于水的杂质) | 水 | 过滤、重结晶 |
| ② | 乙酸乙酯(醋酸) | 氢氧化钠溶液 | 分液 |
| ③ | 乙醇(4%的水) | 生石灰 | 蒸馏 |
| ④ | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| A. | ①② | B. | ①③ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
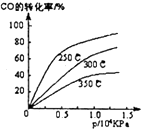 工业合成甲醇反应如下:CO(g)+2H2(g)?CH3OH(g);△H请回答下列问题:
工业合成甲醇反应如下:CO(g)+2H2(g)?CH3OH(g);△H请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
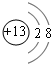
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 在第3周期元素中,C的离子半径简单最小 |
| D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚钠溶液中通入过量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| B. | 溴乙烷的消去反应:C2H5Br+OH-$→_{△}^{水}$C2H4↑+Br-+H2O | |
| C. | 乙醇催化氧化成乙醛:2C2H5OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O | |
| D. | 乙酸乙酯在碱性条件下水解:CH3COOC2H5+H2O?CH3COOH+C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径呈周期性变化 | |
| B. | 元素的化合价呈周期性变化 | |
| C. | 元素的金属性和非金属性呈周期性变化 | |
| D. | 元素原子的核外电子排布呈周期性变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com