
| A. | 液氯 | B. | 氯水 | ||
| C. | NaClO溶液 | D. | Na2O2与水反应后的溶液 |
科目:高中化学 来源: 题型:解答题
 中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g•L-1.某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中
中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g•L-1.某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某饮料公司的广告语为“本公司生产的饮料不含任何化学物质” | |
| B. | 该科研人员发明了一种特殊催化剂,可以使水变为汽油 | |
| C. | 有关部门利用明矾对饮用水进行消毒杀菌,从而解决了灾民饮水难的问题 | |
| D. | 该科研机构发明了一种用植物秸秆生产乙醇的新工艺 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质 | B. | 元素 | C. | 分子 | D. | 氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 形成均匀的无色溶液 | B. | 形成均匀的紫红色溶液 | ||
| C. | 液体分层,上下层均呈无色 | D. | 液体分层,下层呈紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液中c(NH4+)离子浓度 | B. | 氨水的电离程度 | ||
| C. | 水的离子积常数 | D. | c(H+)/c(NH3•H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
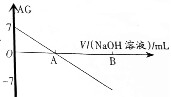 若用AG表示溶液的酸度(acidity grade),AG的定义为AG=lg[$\frac{c({H}^{+})}{c(O{H}^{-})}$].室温下实验室中用0.01mol•L-1的氢氧化钠溶液滴定20.00mL0.01mol•L-1的醋酸,滴定过程如图所示,下列叙述正确的是( )
若用AG表示溶液的酸度(acidity grade),AG的定义为AG=lg[$\frac{c({H}^{+})}{c(O{H}^{-})}$].室温下实验室中用0.01mol•L-1的氢氧化钠溶液滴定20.00mL0.01mol•L-1的醋酸,滴定过程如图所示,下列叙述正确的是( )| A. | 室温下,醋酸的电离常数约为10-6 | |
| B. | A点时加入氢氧化钠溶液的体积为20.00mL | |
| C. | 若B点为40mL,所得溶液中:c(OH-)=c(CH3COO-)+c(H+)+2c(CH3COOH) | |
| D. | 反应过程中一定存在:0.01mol•L-1+c(OH-)=c(Na+)+c(H+)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
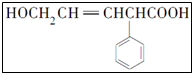 写出该有机物结构中含氧官能团的名称羟基、羧基.
写出该有机物结构中含氧官能团的名称羟基、羧基.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com