
检验SO2中是否混有CO2气体,可采用的方法是( )。
A.通过品红溶液 B.先通过NaOH溶液,再通入澄清石灰水
C.通过澄清石灰水 D.先通过KMnO4酸性溶液,再通过澄清石灰水
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
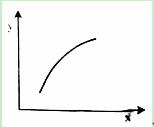
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO,MgSO4(s) + CO(g)  MgO(s) + CO2(g) +SO2(g) △H>0, 该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
MgO(s) + CO2(g) +SO2(g) △H>0, 该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
| 选项 | x | y |
| A | 温度 | 容器内混合气体的密度 |
| B | CO的物质的量 | CO2与CO的物质的量之比 |
| C | SO2的浓度 | 平衡常数K |
| D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为制取纯净干燥的Cl2并让其与铁发生反应的装置,A是Cl2发生装置,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶;烧杯G为尾气吸收装置。
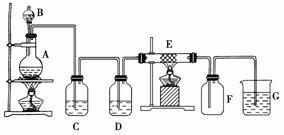
试回答:
(1)C、D、G三个装置所盛放的试剂分别是:
C_____________________________________________________
D___________
G
(2)F中的现象为___________________________,生成物是________。
(3)写出在A、E、G中发生反应的化学方程式为:
A: ;
E: ;
G
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在水溶液中能大量共存的是 ( )
A.Na+、Ba2+、Cl-、SO42- B. Ca2+、HCO3-、C1-、K+
C.Mg2+、Ag+、NO3-、Cl- D. H+ 、Cl- 、Na+ 、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种可溶性盐,它们的阳离子可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子可能是NO3-、SO42-、Cl-、CO32-的某一种。
⑴若把四种盐分别溶解于盛有蒸馏水的四只试管中,只有C盐的溶液呈蓝色;
⑵若向⑴的四只试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味气体逸出。根据⑴⑵实验事实可推断A、B、C、D的化学式各为: ;
写出B、D与盐 酸反应的离子方程式: ;
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.二氧化硫通入石蕊试液中,溶液先变红,后褪色
B.少量二氧化硫通入漂白粉溶液中的化学方程式:SO2+H2O+Ca(ClO)2==CaSO3↓+2HClO
C.亚硫酸钠溶液使溴水褪色的离子方程式:SO32—+H2O+Br2==SO42—+2H++2Br—
D.亚硫酸钠溶液中加入硝酸的离子方程式:SO32—+2H+== SO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
检验SO2中是否混有CO2气体,可采用的方法是( )。
A.通过品红溶液 B.先通过NaOH溶液,再通入澄清石灰水
C.通过澄清石灰水 D.先通过KMnO4酸性溶液,再通过澄清石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
空气质量越来越受到人们的关注,下表是我国部分城市空气质量周报:
| 城市 | 污染指数 | 首要污染物 | 空气质量等级 |
| 太原 | 98 | SO2 | Ⅱ |
| 青岛 | 47 | Ⅰ | |
| 兰州 | 103 | TSP | Ⅲ |
| 广州 | 90 | NOx | Ⅱ |
(注:TSP——总悬浮颗粒物;NOx——氮氧化物)
(1)由上表可知,从理论上分析最容易出现酸雨的城市是________。
(2)悬浮颗粒物不易沉降,它与空气中的SO2、O2接触时,SO2会部分转化为SO3,悬浮颗粒物所起的作用是________(填序号)。
A.氧化剂 B.还原剂 C.催化剂 D.吸附剂
(3)氮的氧化物也是大气污染物之一。目前,治理NO的方法是在一定条件下用氨把一氧化氮还原为氮气和水。科学家又设想,在相同条件下可采用价格比NH3更便宜的天然气来处理NO,达到同样效果,写出该反应的化学方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为达到预期的实验目的,下列操作正确的是( )
A.欲配制量分数为10%的ZnSO4溶液,将10gZnSO4 7H2O溶解在90g水中
7H2O溶解在90g水中
B.欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeC13饱和溶液并长时间煮沸
C.可以使用乙醇提取溴水中的溴单质
D.为鉴别KC1、A1C13和MgC12溶液,各取少量三种溶液分别滴加NaOH溶液至过量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com