
(12分)下图是一个化学过程的示意图。
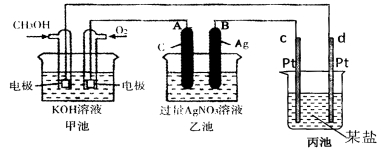
(1)图中乙池是 装置。
(2)c(Pt)电极的名称是 。
(3)写出通入CH3OH电极的电极反应式是 。
(4)乙池中反应的离子方程式为 。
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下);此时丙池某电极析出1.6g某金属,则丙中的某盐溶液可能是 (填序号)
A.MgSO4 B.CuSO4 C.NaCL D.AgNO3
(1)电解或电解池
(2)阳极
(3)CH3OH+8OH--6 e- CO32- +6H2O
(4)4Ag++2H2O 4Ag+O2↑+4H+
4Ag+O2↑+4H+
(5)280 BD
【解析】
试题分析:(1)由图可知甲池能自发发生氧化还原反应,是燃料电池,乙、丙都是电解池装置;
(2)甲池通入甲醇的一极是负极,氧气一极是正极,d与负极相连,所以d是阴极,则c是阳极;
(3)通入甲醇的一极是负极发生氧化反应,失去电子生成二氧化碳,二氧化碳与电解质溶液反应,最终生成碳酸根离子和水,电极反应式为CH3OH+8OH--6 e- CO32- +6H2O;
(4)乙是电解硝酸银溶液,A是阳极,B是阴极,所以阳极产生氧气,阴极产生Ag,离子方程式为4Ag++2H2O 4Ag+O2↑+4H+;
4Ag+O2↑+4H+;
(5)乙中B增加的质量是析出的Ag的质量,所以析出5.4gAg时转移电子的物质的量是5.4g/108g/mol=0.05mol,根据反应O2+4e-+2H2O=4OH-,可知甲池中理论消耗氧气得物质的量是0.05/4mol,标准状况下的体积是0.05/4mol×22.4L/mol=0.28L=280mL;丙池析出金属0.64g,丙池转移电子的物质的量也是0.05mol,若该金属是+1价,则该金属的相对原子质量是1.6/0.05=32,若该金属是+2价金属,则该金属的相对原子质量是1.6/0.05/2=64,所以答案选B。
考点:考查原电池、电解池的判断,电化学原理的应用


科目:高中化学 来源:2014-2015湖南省等三校高一12月联考化学试卷(解析版) 题型:选择题
ClO2是一种杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4 = 2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是
A.KClO3在反应中得到电子
B.ClO2被氧化
C.H2C2O4在反应中被还原
D.1 mol KClO3参加反应有2 mol电子转移
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高一上学期期中考试化学试卷(解析版) 题型:选择题
如果你家里的食用花生油混有较多的水份,你将采用下列何种方法分离
A.过滤 B.蒸馏 C.分液 D.萃取
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高二上学期期中化学(文)试卷(解析版) 题型:选择题
胃酸(盐酸)过多的病人常服用能中和盐酸的药物来治疗,含下列哪种物质的药品达不到治疗效果
A.Al(OH)3 B.CaCO3 C.NaHCO3 D.C6H12O6(葡萄糖)
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高二上学期第三次月考化学试卷(解析版) 题型:选择题
有①甲烷、②乙烯、③苯、④聚乙烯、⑤丙炔、⑥环己烷、⑦邻二甲苯、⑧环己烯(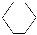 )。其中既能使KMnO4酸性溶液褪色又能与溴水反应使溴水褪色的是
)。其中既能使KMnO4酸性溶液褪色又能与溴水反应使溴水褪色的是
A.②④⑤⑧ B.②⑤⑧ C.②④⑤⑦ D.②④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高二上学期第三次月考化学试卷(解析版) 题型:选择题
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1 mol时,下列说法不正确的是
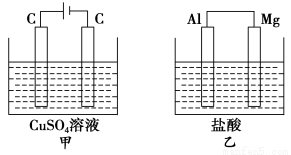
A.溶液的质量变化:甲减小乙增大
B.溶液pH变化:甲减小乙增大
C.相同条件下产生气体的体积:V甲=V乙
D.电极反应式:甲中阴极为Cu2++2e-===Cu,乙中负极为Mg-2e-===Mg2+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期第四次月考化学试卷(解析版) 题型:选择题
常温下,不可能与NaHCO3溶液反应生成气体的物质是
A.酸 B.碱 C.盐 D.氧化物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.已知 则可以计算CH3—CH3 → CH2=CH2+H2;ΔH =+125.6 kJ/mol
则可以计算CH3—CH3 → CH2=CH2+H2;ΔH =+125.6 kJ/mol
B.能说明NH3结合H+能力比H2O强:NH3+H3O+=NH+4+H2O
C.已知下列热化学方程式:2H2(g)+O2(g) === 2H2O(g) △H=-484kJ/mol,则氢气的燃烧热为-242kJ/mol
D.已知中和热为-57.4kJ/mol ,则NaOH(aq) +CH3COOH(aq)=CH3COONa(aq)+H2O(l);△H =-57.4kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com