
| A. | 丙醛 | B. | 丙烯醛 | C. | 甲醛 | D. | 丁烯醛 |
分析 n(Ag)=$\frac{4.32g}{108g/mol}$=0.04mol,-CHO发生银镜反应时醛基和Ag的物质的量之比为1:2,则生成4.32gAg需要该醛的物质的量为$\frac{1}{2}$n(Ag)=$\frac{1}{2}$×0.04mol=0.02mol,等质量的该醛完全燃烧后生成n(H2O)=$\frac{1.08g}{18g/mol}$=0.06mol,根据H原子守恒得n(H)=2n(H2O)=2×0.06mol=0.12mol,则醛分子个数与H原子个数之比等于其物质的量之比=0.02mol:0.12mol=1:6;
若为甲醛,-CHO发生银镜反应时醛基和Ag的物质的量之比为1:4,则生成4.32gAg需要该醛的物质的量为0.01mol,n(H2O)=$\frac{1.08g}{18g/mol}$=0.06mol,根据H原子守恒得n(H)=2n(H2O)=2×0.06mol=0.12mol,则醛分子个数与H原子个数之比等于其物质的量之比=0.01mol:0.12mol=1:12,以此来解答.
解答 解:n(Ag)=$\frac{4.32g}{108g/mol}$=0.04mol,若为甲醛,-CHO发生银镜反应时醛基和Ag的物质的量之比为1:4,则生成4.32gAg需要该醛的物质的量为0.01mol,n(H2O)=$\frac{1.08g}{18g/mol}$=0.06mol,根据H原子守恒得n(H)=2n(H2O)=2×0.06mol=0.12mol,则醛分子个数与H原子个数之比等于其物质的量之比=0.01mol:0.12mol=1:12,不符合;
若为其它一元醛,-CHO发生银镜反应时醛基和Ag的物质的量之比为1:2,则生成4.32gAg需要该醛的物质的量为$\frac{1}{2}$n(Ag)=$\frac{1}{2}$×0.04mol=0.02mol,等质量的该醛完全燃烧后生成n(H2O)=$\frac{1.08g}{18g/mol}$=0.06mol,根据H原子守恒得n(H)=2n(H2O)=2×0.06mol=0.12mol,则醛分子个数与H原子个数之比等于其物质的量之比=0.02mol:0.12mol=1:6;说明该醛分子中含有6个H原子,符合条件的有AD,
故选AD.
点评 本题考查有机物的计算,为高频考点,明确醛发生银镜反应时醛和Ag的物质的量之比是解本题关键,注意原子守恒的灵活运用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
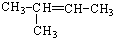 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的颜色逐渐变浅 | |
| B. | 气态氢化物的稳定性逐渐增强 | |
| C. | 从F→I,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次减弱 | |
| D. | 单质的熔沸点逐渐降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
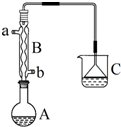 正溴丁烷(CH3CH2CH2CH2Br)是一种重要的有机合成工业原料.在实验中可利用下图装置(加热或夹持装置省略)制备正溴丁烷.制备时的化学反应方程式及有关数据如下:
正溴丁烷(CH3CH2CH2CH2Br)是一种重要的有机合成工业原料.在实验中可利用下图装置(加热或夹持装置省略)制备正溴丁烷.制备时的化学反应方程式及有关数据如下:| 物质 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 水中溶解性 |
| 正丁醇 | 74 | 0.80 | 117.3 | 微溶 |
| 正溴丁烷 | 137 | 1.27 | 101.6 | 难溶 |
| 溴化氢 | 81 | --- | --- | 极易溶解 |
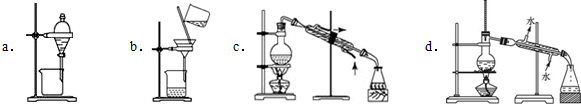
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,23 g NO2和N2O4的混合气体中含有NA个氧原子 | |
| B. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA | |
| C. | 7.1gCl2与足量的氢氧化钠溶液反应转移的电子数为0.2NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com