
п�̸ɵ�������Ĺ���������ڷ�������뻷���н��������Σ�����ԷϾɵ�ؽ�����Դ�������Ե÷dz���Ҫ��ij��ѧ��ȤС����������´����������շϵ���еĸ�����Դ��
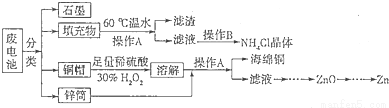
��1������п�̸ɵ�صĵ����ΪKOH���ܷ�ӦΪZn+2MnO2+2H2O=2MnOOH+Zn(OH)2���为���ĵ缫��ӦʽΪ ��
��2���������60����ˮ�ܽ⣬Ŀ���Ǽӿ��ܽ����ʣ�����������¶Ȳ���̫�ߣ���ԭ���� ��
��3������A������Ϊ ��
��4����������Ҫ�ɷ�Ϊ���̻������̻�����м���һ������ϡ���ᡢϡ���ᣬ�����Ͻ�����������Ϊֹ������Ҫ��ӦΪ2MnO(OH)+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2+6H2O��
�ٵ�1 mol MnO2�μӷ�Ӧʱ������ mol���ӷ���ת�ơ�
��MnO(OH)��Ũ�����ڼ���������Ҳ�ɷ�����Ӧ����д���䷴Ӧ�Ļ�ѧ����ʽ ��
��5��ͭñ�ܽ�ʱ����H2O2��Ŀ���� ���û�ѧ����ʽ��ʾ����ͭñ�ܽ���ȫ�ɲ���_______������ȥ��Һ�й�����H2O2��
��6��п�̸ɵ�������Ĺ�����KMnO4��Һ���ա��ڲ�ͬpH�£�KMnO4��Һ��Hg�������ʼ���Ҫ��������ͼ��ʾ��

������ͼ��֪��
��pH��Hg�����ʵ�Ӱ������� ��
����ǿ���Ի�����Hg�������ʸߵ�ԭ������� ��
��1��Zn+2OH��-2e��=Zn(OH)2
��2���¶ȹ����Ȼ�����ȷֽ⣻
��3������
��4����4 ��2MnO(OH)+6HCl��Ũ��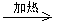 2MnCl2+Cl2��+4H2O
2MnCl2+Cl2��+4H2O
��5��Cu+H2O2+H2SO4=CuSO4+2H2O ����
��6��������pH���������������ȼ�С������
�ڸ������������������������ǿ
����������1����������������Ӧ���ɷ���ʽ��֪Zn����������Zn(OH)2����缫����ʽΪZn+2OH��-2e��=Zn(OH)2��
��2���ϸ��¶�ʱ���Ȼ���ֽ������Ȼ���Ͱ��������Եò����Ȼ�茶��塣
��3�����벻���Թ������Һ���ù��˵ķ��������Ըò��������ǹ��ˡ�
��4����������Ҫ�ɷ�Ϊ���̻������̻�����м���һ������ϡ���ᡢϡ���ᣬ�����Ͻ�����������Ϊֹ������Ҫ��ӦΪ2MnO(OH)+MnO2+2H2C2O4+3H2SO4�T3MnSO4+4CO2��+6H2O��
�ٸ÷�Ӧ�У���������MnO(OH)��MnO2����ԭ���Dz��ᣬ��1mol MnO2�μӷ�Ӧʱ��ת�Ƶ��ӵ����ʵ���=1mol��2��2��(4?3)=4mol��
��MnO(OH)��Ũ�����ڼ���������Ҳ�ɷ�����Ӧ�����Ȼ��̡�������ˮ����Ӧ����ʽΪ��MnO(OH)+6HCl��Ũ��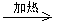 2MnCl2+Cl2��+4H2O��
2MnCl2+Cl2��+4H2O��
��5�����������£�˫��ˮ�ܽ�ͭ��������ͭ���ӷ�Ӧ�Ļ�ѧ����ʽΪ��
Cu+H2O2+H2SO4=CuSO4+2H2O�����������£�˫��ˮ�ֽ�����ˮ�����������Գ�ȥ˫��ˮ�ķ����Ǽ��ȣ�
��6���ٸ���ͼ��֪������pH���������������ȼ�С���������������£�������ؾ���ǿ�����ԣ��������������µĸ�����������Ը�ǿ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��16 ���ͣ������
ǰ������ԭ���������������Ԫ��A��B��C��D�У�A��B�ļ۵��Ӳ���δ�ɶԵ��Ӿ�ֻ��1����ƽ��A����B+�ĵ������Ϊ8����Bλ��ͬһ���ڵ�C��D�����Ǽ۵��Ӳ��е�δ�ɶԵ������ֱ�Ϊ4��2����ԭ���������Ϊ2��
�ش��������⣺
��1��D2+�ļ۲�����Ų�ͼΪ_______��
��2������Ԫ���е�һ������С����________���縺��������________������Ԫ�ط��ţ�
��3��A��B��D����Ԫ����ɵ�һ��������ľ�����ͼ��ʾ��
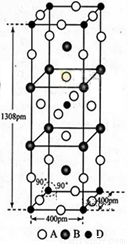
�ٸû�����Ļ�ѧʽΪ_________________��D����λ��Ϊ___________��
����ʽ����þ�����ܶ�_______g��cm-3��
��4��A-��B+��C3+����������ɵĻ�����B3CA6�����л�ѧ����������_________���û������д���һ���������ӣ������ӵĻ�ѧʽΪ________����λ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��15 ���ͣ�ѡ����
Ϊ�ⶨijþ���Ͻ���Ʒ�����ĺ���������������ʵ�飺ȡһ�����Ͻ𣬼���100 mL 0.3 mol��L��1ϡ���ᣬ�Ͻ���ȫ�ܽ⣬�����������ڱ�״�������Ϊ560 mL���ټ���0.2 mol��L��1 NaOH��Һ����������ǡ�ò��ٱ仯����ȥ350 mL NaOH��Һ������ȡ��Ʒ���������ʵ���Ϊ
A��0.005 mol
B��0.010 mol
C��0.020 mol
D��0.030 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��14 ���ͣ�ѡ����
���л�ѧ���������ȷ���ǣ� ��
A��CH3COONH4�ĵ��뷽��ʽΪ: CH3COONH4 CH3COO-+NH4+
CH3COO-+NH4+
B��NaHS��ˮ�ⷽ��ʽΪ: HS-+H2O S2-+H3O+
S2-+H3O+
C���ù����İ�ˮ����SO2�����ӷ���ʽΪ: 2NH3��H2O+SO2��2NH4++SO32-+H2O
D������Fe����Cl2��Ӧ�Ļ�ѧ����ʽΪ: Fe +Cl2FeCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��14 ���ͣ�ѡ����
����ѡ���е�ͼ������ʾ����������Ӧ��Ӧ���ϵ���(a��b��c��d������0)
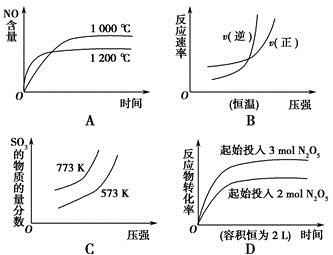
A��4NH3(g)��5O2(g)  4NO(g)��6H2O(g) ��H����a kJ��mol��1
4NO(g)��6H2O(g) ��H����a kJ��mol��1
B��N2(g)��3H2(g)  2NH3(g)����H����b kJ��mol��1
2NH3(g)����H����b kJ��mol��1
C��2SO3(g)  2SO2(g)��O2(g)����H����c kJ��mol��1
2SO2(g)��O2(g)����H����c kJ��mol��1
D��2N2O5(g)  4NO2(g)��O2(g) ��H����d kJ��mol��1
4NO2(g)��O2(g) ��H����d kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��13 ���ͣ������
���л��ﻯѧ������
ƻ����㷺������ƻ����ˮ���Ĺ����У���һ�ֳ��õ�ʳƷ���Ӽ������ⶨ��ƻ�������Է�������Ϊ134��������Ԫ�ص���������Ϊ��w(c)=35.82% W(H)=4.86%,����Ϊ�������д���5�ֲ�ͬ��ѧ������Hԭ�ӡ�1molƻ��������2molNaHCO3��ȫ��Ӧ������������Na��Ӧ����1.5molH2�ġ�����ϩΪԭ���˹��ϳ�ƻ�������·���£�
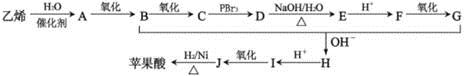
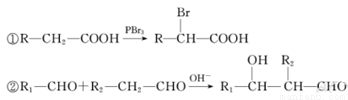
��֪��
��ش��������⣺
��1��ƻ����ķ���ʽΪ_______��A���ʵ�����Ϊ_______��
��2��F�к��еĹ�����������_______��G+B��H�ķ�Ӧ������_______��
��3���ںϳ���·�У�C��D��һ���跴Ӧ��Ŀ����_____��
��4��D��E��Ӧ�Ļ�ѧ����ʽΪ_________��
��5��ƻ�����NaHCO3��ȫ��Ӧ�Ļ�ѧ����ʽΪ________��
��6����ƻ���Ậ����ͬ����������Ĺ����ŵ�ͬ���칹��Ľṹ��ʽΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��13 ���ͣ�ѡ����
�����±���CuFeS2�ķ�Ӧ֮һΪ2CuFeS2+7O2=CuSO4+CuO+Fe2O3+3SO2�����й��ڸ÷�Ӧ��������ȷ����
A��CuFeS2����Ļ��ϼ�Ϊ-1
B��CuFeS2������ԭ��Ӧ
C��1 mol CuFeS2��ȫ��Ӧת��13 mol����
D��CuSO4��SO2��������������ǻ�ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��12 ���ͣ�ѡ����
���и������ӿ��ܴ����������
A����ʹ�⻯�ص�����ֽ��������Һ��Na����NH��S2����Br��
B����pH��ֽ���ɫ����Һ��Fe2+��S2O��SO42����Na+
C��ˮ�������c(H��) ?c(OH��) =10��28����Һ��Na����S2����NO3�� ��SO32 ��
D����ʹKSCN�Ժ�ɫ����Һ��Na����NH4����AlO��CO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��10 ���ͣ�ѡ����
��ͼΪԪ�����ڱ������ڵ�һ����,Eԭ�ӵĵ��Ӳ���Ϊn������������Ϊ2n+1����������ȷ����
A |
| B | C |
|
| D | E |
A��C��E�⻯������ȶ��Ժͻ�ԭ�Ծ����μ���
B��A��B�γɵ������ӿ�����AB32�� A2B42��
C��AD2������ÿ��ԭ�ӵ�������Ϊ8���ӽṹ
D��A��D��E������������Ӧ��ˮ���������������ǿ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com