
25 ℃、101 kPa下:①2Na(s)+  O2(g)===Na2O(s);ΔH1=-414 kJ/mol
O2(g)===Na2O(s);ΔH1=-414 kJ/mol
②2Na(s)+O2(g)===Na2O2(s);ΔH2=-511 kJ/mol
下列说法正确的是
A.①和②产物中的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25 ℃、101 kPa下,Na2O2(s)+2Na(s)===2Na2O(s) ; ΔH=-317 kJ/mol
科目:高中化学 来源:2014-2015安徽省淮南市高一上学期期末考试化学试卷(解析版) 题型:选择题
某学生用氯气消毒的自来水配制下列物质的溶液,不会产生明显的药品变质问题的是
A.AgNO3 B.AlCl3 C.Na2CO3 D.FeCl2
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(文)试卷(解析版) 题型:选择题
某人在检查身体时,发现尿液呈酸性,医生建议他少吃下列食物中的
A.苹果 B.肉类食物 C.菠菜 D.海带
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(理)试卷(解析版) 题型:填空题
请仔细观察两种电池的构造示意图,

回答下列问题:
(1)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,
则负极的电极反应式: 。
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其可能的原因是 。
(3)原电池可将化学能转化为电能。某课外活动小组设计两种类型的原电池,以 探究其能量转化效率。
限选材料:ZnSO4(aq), CuSO4(aq);铜片,锌片和导线。
①完成原电池甲的装置示意图(见下图),并作相应标注。
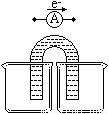
(要求:在同一烧杯中,电极与溶液含相同的金属元素)
②组装原电池乙,要求:以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中,工作一段时间后,可观察到负极 。
③甲乙两种原电池中可更有效地将化学能转化为电能的是 ,(填“甲”或“乙”),其原因是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
硫化钠(Na2S)的水溶液中存在着多种微粒,下列关系正确的是
A.c(OH-)= c(HS-)+c(H+)+c(H2S) B.c(OH-) = c(HS-)+c(H+)+2 c(H2S)
C.c(Na+) = c(S2-)+c(HS-) +c(H2S) D.c(Na+)+c (H+)= c(HS-)+c(OH-)+c(S2-)
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
下列说法错误的是
A.升高温度可使吸热反应的反应速率增大,使放热反应的反应速率减小
B.决定化学反应速率的主要因素是参加反应的物质的性质
C.对于有气体参加的反应,增大压强,反应速率加快
D.催化剂能增大单位体积内活化分子的百分数,从而增大化学反应速率
查看答案和解析>>
科目:高中化学 来源:2014-2015重庆市高二上学期第二次月考化学试卷(解析版) 题型:填空题
(1)请写出下列溶液的离子反应方程式:(13分)
①硫酸氢钠在溶液中的电离:
②氯化铵溶液除铁锈的原因:
③氯化铁溶液与偏铝酸钾溶液混合:
④碳酸钙的溶解平衡:
(2)在配制AgNO3溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,
以 (填“促进”、“抑制”)其水解。在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产是 。把Na2SO3溶液蒸干,灼烧,最后得到的主要固体产是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西岐山县高一上学期期末质量检测化学试卷(解析版) 题型:选择题
下列化学方程式中,能用离子方程式:Ba2+ + SO42- = BaSO4↓表示的是
A.Ba(OH)2 + (NH4)2SO4 == BaSO4↓ + 2NH3H2O
B.Ba(OH)2 + H2SO4 == BaSO4↓ + 2H2O
C.BaCO3 + H2SO4 == BaSO4↓ + 2H2O + CO2↑
D.BaCl2 + Na2SO4 == BaSO4↓ + 2NaCl
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省弥勒市高三市统测一模理综化学试卷(解析版) 题型:填空题
选考【化学---选修2:化学与技术(15分)】
MgSO4·7H2O在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-一硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
表2 两种盐的溶解度(单位为g/100g水)
温度/ ℃ | 10 | 30 | 40 | 50 | 60 |
CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |
硼镁泥制取七水硫酸镁的工艺流程如下:
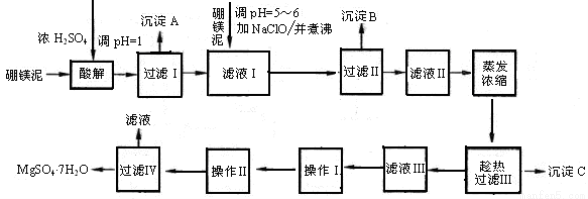
根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)沉淀C的化学式是
(2)过滤Ⅲ需趁热过滤的理由是
(3)操作Ⅰ和操作Ⅱ的名称分别为 、
(4)滤液I中加入硼镁泥,调节溶液的pH=5~6,可除去滤液Ⅰ中 (填离子符号);加入NaClO溶液加热煮沸,可将Fe2+氧化成Fe3+的同时,还会将溶液中的Mn2+氧化成MnO2,写出Mn2+被氧化成MnO2的离子反应方程式为
(5)硼镁泥是硼镁矿生产硼砂(Na2B4O7·10H2O)时的废渣。将硼镁矿(Mg2B2O5·H2O)煅烧、粉碎后加水和纯碱,在加热加压下通入CO2可得硼砂。此反应为熵减小反应,试写出反应方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com