
下列有关化学用语表示正确的是( )
A.次氯酸的电子式 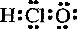
B.S2-的结构示意图: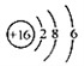
C.质子数为53,中子数为78的碘原子:13153I
D.NH4I的电子式: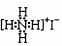
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届江西省高三5月月考理综化学试卷(解析版) 题型:选择题
在固态金属氧化物电解池中,高温共电解H2O﹣CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
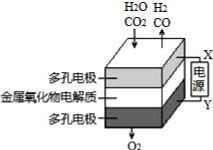
A.X是电源的负极
B.阴极的反应式是:H2O+2e﹣═H2+O2﹣,CO2+2e﹣═CO+O2﹣
C.总反应可表示为:H2O+CO2 H2+CO+O2
H2+CO+O2
D.阴、阳两极生成的气体的物质的量之比是1:1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江双鸭山一中高二下期中化学试卷(解析版) 题型:选择题
下列四个反应中,与其它三个反应类型不同的是( )
A CH3CHO+H2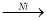 CH3CH2OH
CH3CH2OH
B CH3CHO+2Ag(NH3)2OH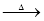 CH3COONH4+2Ag↓+3NH3+H2O
CH3COONH4+2Ag↓+3NH3+H2O
C CH3CHO+2Cu(OH)2+NaOH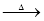 CH3COONa+Cu2O↓+3H2O
CH3COONa+Cu2O↓+3H2O
D 2CH3CHO+O2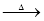 2CH3COOH
2CH3COOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高一下期中化学试卷(解析版) 题型:选择题
已知五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。下列说法正确的是( )
A.D元素最高价氧化物对应的水化物化学式H2YO4
B.原子半径由大到小的顺序为:B>D> E
C.B、C两种元素的气态氢化物中,C的气态氢化物较稳定
D.A与B形成的两种化合物中,阴、阳离子物质的量之比均为1:2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高一下期中化学试卷(解析版) 题型:选择题
与氢氧根离子具有相同的质子数和电子数的微粒是( )
A.CH4 B.NH4+ C.NH2- D.Cl-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二下期中化学试卷(解析版) 题型:推断题
已知: 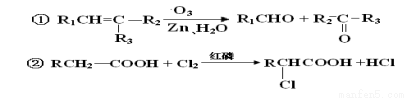
有如下转化关系,E能发生银镜反应,F为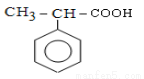 。
。
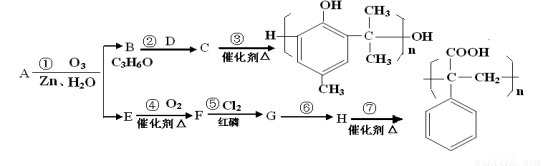
请填写下列空白:
(1)写出下列物质的结构简式:A ;E 。
(2)D的同分异构体中属于芳香族化合物的有 种(D除外),其中不与Na反应的是 (结构简式)。
(3)写出下列反应的反应类型:③ ,⑥ 。
(4)写出E和新制的Cu(OH)2悬浊液反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二下期中化学试卷(解析版) 题型:选择题
有关右图所示物质的下列叙述中,正确的是( )
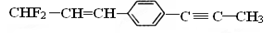
A.所有原子共面
B.12个碳原子不可能共平面
C.除苯环外的其余碳原子不可能共直线
D.除苯环外的其余碳原子可能共直线
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东实验中学高二下期中化学试卷(解析版) 题型:简答题
2013年诺贝尔化学奖授予三位美国科学家,以表彰他们如光合作用叶绿体光反应时酶中、生物固氮时固氮酶中)的化学反应。
(1)固氮酶有铁蛋白和钒铁蛋白两种,它们不仅能够催化N2还原成NH3,还能将环境底物乙炔催化还原成乙烯,下列说法正确的有________(不定项选择)。
a.每个C2H2和C2H4分子中的π键数目相同 b.碳负离子CH呈三角锥形
c. NO+电子式为 [∶N??O∶]+ d.NH3沸点比N2高,主要是因为前者是极性分子
(2)钒可合成电池电极,也可人工合成二价钒(V)固氮酶(结构如图)
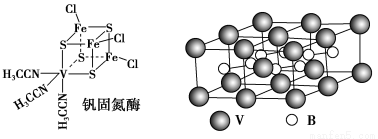
V元素位于周期表的______区,该原子基态时的价层电子排布式为___________________。
②钒固氮酶中钒的配位原子有________(写元素符号)。
③熔融空气电池钒硼晶体晶胞结构如图所示,该晶胞中含有钒原子数目为________。
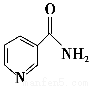
(3)烟酰胺(结构简式如图)可用于合成光合辅酶NADPH,烟酰胺分子中氮原子的杂化轨道类型有 ,1 mol该分子中含σ键的数目为______________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:填空题
下图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336 mL(标准状况)气体。回答:

(1)直流电源中,M为____________极。
(2)Pt电极上生成的物质是____________,其质量为____________g。
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为:2∶_______∶________∶_________。
(4)AgNO3溶液的浓度(填“增大”“减小”或“不变”。下同)____________,H2SO4溶液的浓度____________。
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为______g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com