
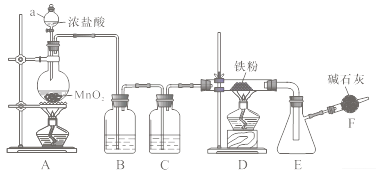
【题目】无水三氯化铁是有机合成的催化剂,为棕黄色固体,易潮解产生白雾,300℃左右时升华。实验室可用氯气与铁反应制备无水三氯化铁,下图是甲组学生设计的制备装置。
回答下列问题:
(1)仪器a的名称是________;装置B的作用是_________,C中盛装试剂是______。
(2)装置D中发生反应的化学方程式为___________________。
(3)装置D与E之间不用玻璃导气管连接,原因是_________;点燃装置D处酒精灯的时机是_______。
(4)装置F的作用是_____________。
(5)与甲组设计对比,乙组同学去掉了装置C。实验时无论怎样改变铁粉的用量,装置D中都有少量的黑色固体残留。乙组同学猜测该黑色固体可能是__________,其依据是(用化学方程式表示)________,验证该猜测的实验方法是________。
【答案】分液漏斗 除去氯气中的HCl 浓硫酸 2Fe+3Cl2![]() 2FeCl3 防止FeCl3冷凝成固体堵塞玻璃导管 待D装置的玻璃管内充满黄绿色气体时再点燃酒精灯 吸收尾气防止污染空气,同时防止空气中的水蒸气进入装置E中 Fe3O4 3Fe+4H2O(g)
2FeCl3 防止FeCl3冷凝成固体堵塞玻璃导管 待D装置的玻璃管内充满黄绿色气体时再点燃酒精灯 吸收尾气防止污染空气,同时防止空气中的水蒸气进入装置E中 Fe3O4 3Fe+4H2O(g)![]() Fe3O4+4H2 取少量该固体,用磁铁(或铁片)靠近,若发生吸引,则推测成立(或其他合理答案)
Fe3O4+4H2 取少量该固体,用磁铁(或铁片)靠近,若发生吸引,则推测成立(或其他合理答案)
【解析】
在装置A中浓盐酸与MnO2混合加热制取Cl2,由于浓盐酸具有挥发性,制取的Cl2中含有HCl和水蒸气,装置B中饱和食盐水用于除去HCl,装置C中浓硫酸进行Cl2的干燥,在装置D中Fe与Cl2反应产生FeCl3,在装置E中收集FeCl3,为防止Cl2污染大气,同时防止FeCl3潮解,在E支管处连接一个盛有碱石灰的干燥管,用以吸收Cl2及空气中的水蒸气。
(1)根据装置图可知仪器a名称为分液漏斗;装置B中盛有饱和食盐水,作用是除去氯气中的HCl;装置C中盛有浓硫酸,作用是干燥Cl2;
(2)在装置D中Fe与Cl2在加热条件下发生反应产生FeCl3,反应方程式为:2Fe+3Cl2![]() 2FeCl3;
2FeCl3;
(3)装置D与E之间不用玻璃导气管连接,是由于FeCl3蒸气冷凝变成固体时容易发生堵塞玻璃导管现象,所以就不使用导气管,直接进入收集装置锥形瓶E中;为防止Fe粉与装置中空气里含有的氧气发生反应,应该在D装置的玻璃管内充满黄绿色气体时再点燃酒精灯;
(4)装置F是盛有碱石灰的干燥管,其作用是吸收尾气中的未反应的Cl2,防止污染空气,同时防止空气中的水蒸气进入装置E中;
(5)若不使用浓硫酸干燥Cl2,在加热时Fe与空气中的H2O蒸气发生反应产生Fe3O4和H2,反应方程式为:3Fe+4H2O(g)![]() Fe3O4+4H2;Fe3O4俗称磁性氧化铁,能够被磁铁吸引,也能吸引金属铁,所以证明发生该反应的实验方法是取少量该固体,用磁铁(或铁片)靠近,若发生吸引,则推测成立。
Fe3O4+4H2;Fe3O4俗称磁性氧化铁,能够被磁铁吸引,也能吸引金属铁,所以证明发生该反应的实验方法是取少量该固体,用磁铁(或铁片)靠近,若发生吸引,则推测成立。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知:![]() H<0,将一定量的
H<0,将一定量的![]() 充入注射器中密封,测定气体透光率,并压缩注射器,气体透光率随时间的变化如图
充入注射器中密封,测定气体透光率,并压缩注射器,气体透光率随时间的变化如图![]() 气体颜色越深,透光率越小
气体颜色越深,透光率越小![]() 。下列说法正确的是
。下列说法正确的是
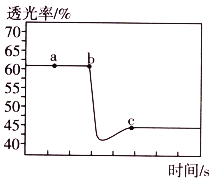
A.a点时化学反应速率为0
B.c点:υ正(NO2)>υ逆(NO2)
C.b点与c点相比,c(NO2)增大,c(N2O4)减小
D.若容器绝热,则平衡常数![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳经济”备受关注,研究和深度开发![]() 的应用对构建生态文明社会具有重要的意义。
的应用对构建生态文明社会具有重要的意义。

(1)![]() 是一种性能优良的光催化剂,能有效地将有机污染物转化为
是一种性能优良的光催化剂,能有效地将有机污染物转化为![]() 等小分子物质。图1为在
等小分子物质。图1为在![]() 的催化下,
的催化下,![]() 降解
降解![]() 的示意图,则该反应的化学方程式为____________________________。
的示意图,则该反应的化学方程式为____________________________。
(2)将一定量的![]() 和
和![]() 通入一恒容密闭容器中发生反应:
通入一恒容密闭容器中发生反应:![]() 。
。
![]() 化学链燃烧技术是目前能源领域研究的热点之一,用NiO作载氧体的化学链燃烧的相关热化学方程式如下:
化学链燃烧技术是目前能源领域研究的热点之一,用NiO作载氧体的化学链燃烧的相关热化学方程式如下:
![]()
![]()
则反应![]() 的
的![]() _______。
_______。
![]() 为了探究反应
为了探究反应![]() 的反应速率与浓度的关系,起始时向恒容密闭容器中通入
的反应速率与浓度的关系,起始时向恒容密闭容器中通入![]() 与
与![]() ,并使二者物质的量浓度均为
,并使二者物质的量浓度均为![]() ,平衡时,根据相关数据绘制出两条反应速率与浓度关系曲线
,平衡时,根据相关数据绘制出两条反应速率与浓度关系曲线![]() 如图
如图![]() :
:![]() 和
和![]() 。则与曲线
。则与曲线![]() 相对应的是图中曲线________
相对应的是图中曲线________![]() 填“甲”或“乙”
填“甲”或“乙”![]() ;该反应达到平衡后,某一时刻降低温度,反应重新达到平衡,则此时曲线甲对应的平衡点可能为________
;该反应达到平衡后,某一时刻降低温度,反应重新达到平衡,则此时曲线甲对应的平衡点可能为________![]() 填字母
填字母![]() 。
。
(3)用稀氨水喷雾捕集![]() 最终可得产品
最终可得产品![]() 。
。
![]() 在捕集时,气相中有中间体
在捕集时,气相中有中间体![]() 氨基甲酸铵
氨基甲酸铵![]() 生成。现将一定量纯净的氨基甲酸铵置于恒容密闭真空容器中,分别在不同温度下进行反应:
生成。现将一定量纯净的氨基甲酸铵置于恒容密闭真空容器中,分别在不同温度下进行反应:![]() 。实验测得的有关数据如下表
。实验测得的有关数据如下表![]() :
:

氨基甲酸铵的分解反应是________![]() 填“放热”或“吸热”
填“放热”或“吸热”![]() 反应。在
反应。在![]() ,此反应的化学平衡常数
,此反应的化学平衡常数![]() ________。
________。
![]() 在
在![]() 溶液中,反应
溶液中,反应![]() 的平衡常数
的平衡常数![]() 。已知常温下
。已知常温下![]() 的电离平衡常数
的电离平衡常数![]() ,则
,则![]() 的电离平衡常数
的电离平衡常数![]() ________。
________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在体积为2 L的密闭容器中,气态物质A、B、E、F的物质的量n随时间t的变化情况如图甲所示,在一定条件下反应达到平衡状态,反应进程中正反应速率随时间的变化情况如图乙所示,在t2、t4时刻分别只改变一个条件(温度、压强或某反应物的量)。下列说法错误的是( )
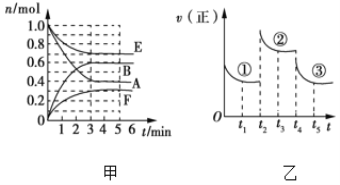
A. 此温度下,该反应的化学方程式为2A(g)+E(g)![]() 2B(g)+F(g)
2B(g)+F(g)
B. 若平衡状态①和②对应的温度相同,则①和②对应的平衡常数K一定相同
C. t2时刻改变的条件是增大压强
D. t4时刻改变的条件是降低温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是原子序数依次增大的第二、三周期主族元素,A、B、C的单质(用a、b、c表示)及其化合物x、y、z有如下转化关系,D与B同主族,下列说法正确的是

A. x、y、z均是离子化合物
B. 简单氢化物的沸点:C﹥B﹥D
C. 最高价氧化物对应的水化物的酸性:A﹥D
D. 简单离子半径:D﹥C﹥B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)煤的利用可以是直接燃烧,也可以是先气化再燃烧 ,下面用等量的C分别按两途径进行反应
a. C(s)+O2(g) = CO2(g) △H =E1
b. C(s) +H2O(g)=CO(g)+H2 (g) △H =E2
H2(g)+![]() O2(g)=H2O(g ) △H =E3
O2(g)=H2O(g ) △H =E3
CO(s)+![]() O2(g)=CO2(g) △H =E4
O2(g)=CO2(g) △H =E4
甲同学认为:煤的气化效率高,所以b途径产生的热量高。乙同学认为,a、b途径产生的热量在理论上应该相同,你认为_____同学说法正确,理由是______________。
(2)在一元强碱MOH溶液中加入一元酸HA溶液,充分反应后,溶液呈中性。甲同学认为溶液中c(A-)=c(M+),而乙同学认为c(A-)是否等于 c(M+),要看一元酸HA是强酸还是弱酸。你认为_____同学说法正确,理由是______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法正确的是( )
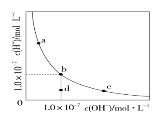
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl3可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式为C8H8O2,A的核磁共振氢谱如图,峰面积之比为1:2:2:3,A分子中只含一个苯环,且苯环上只有一个取代基,其核磁共振氢谱与红外光谱如图。关于A的下列说法中不正确的是
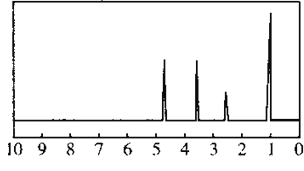
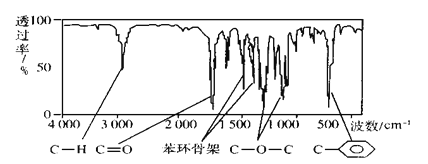
A.A分子属于酯类化合物,在一定条件下能发生水解反应
B.A在一定条件下可与3mol H2发生加成反应
C.符合题中A分子结构特征的有机物只有一种
D.与A属于同类化合物的同分异构体只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示。则下列有关说法不正确的是
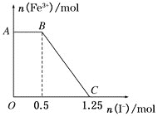
A.图中AB段主要是高锰酸钾和碘化钾溶液反应
B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2
C.根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25 mol
D.根据OC段的数据可知开始加入的硫酸亚铁的物质的量为1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com