
| A. | 甲、乙、丙中均一定含有离子键 | |
| B. | 丙中元素Y可用AgNO3溶液直接检验 | |
| C. | 离子半径大小为X2-<Y-<Z+ | |
| D. | 酸性条件下,丙的氧化性一定比乙强 |
分析 室常温下,Y的单质与常见的一元强碱溶液反应,可得到甲和乙,甲、乙、丙三种化合物中均含有元素Y和Z,说明Y中元素在碱中发生了歧化反应,常温下能与碱溶液发生歧化反应的在中学化学中主要是S、Cl2、Br2等,化合物丙受热催化分解可得甲和X的单质,可知应为KClO3分解,由此可知X为O元素,Y为Cl元素,Z为K元素,A为Cl2,丙为KClO3,甲为KCl,乙为KClO,验证符合题意,据此解答.
解答 解:室常温下,Y的单质与常见的一元强碱溶液反应,可得到甲和乙,甲、乙、丙三种化合物中均含有元素Y和Z,说明Y中元素在碱中发生了歧化反应,常温下能与碱溶液发生歧化反应的在中学化学中主要是S、Cl2、Br2等,化合物丙受热催化分解可得甲和X的单质,可知应为KClO3分解,由此可知X为O元素,Y为Cl元素,Z为K元素,A为Cl2,丙为KClO3,甲为KCl,乙为KClO,验证符合题意.
A.甲为KCl,乙为KClO,丙为KClO3,均含有离子键,故A正确;
B.丙为KClO3,没有氯离子,不能用AgNO3溶液直接检验,故B错误;
C.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径大小为O2-<K+<Cl-,故C错误;
D.酸性条件下,KClO3的氧化性比较KClO弱,故D错误,
故选:A.
点评 本题考查元素化合物推断,学生综合利用题中信息、结合物质性质,猜测出一些物质C12、KC1O3等,再顺推、逆推和逐个验证判断,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 食用油不宜长时间高温反复使用 | |
| B. | 汽车尾气中的NO是氮气和氧气在高温下反应产生的 | |
| C. | 门窗玻璃和玛瑙手镯所用材料的主要成分都是硅酸盐 | |
| D. | 不锈钢在空气中非常稳定,是因为不锈钢表面形成了一层很薄的含铬氧化物致密膜,有效地保护内层金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
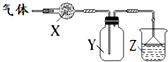 如图装置用于气体的干燥、收集和尾气吸收,其中X、Y、Z对应都正确的是( )
如图装置用于气体的干燥、收集和尾气吸收,其中X、Y、Z对应都正确的是( )| X | Y | Z | |
| A | 无水硫酸铜 | 氯气 | 饱和食盐水 |
| B | 碱石灰 | 氨气 | 水 |
| C | 氯化钙 | 二氧化硫 | 氢氧化钠 |
| D | 氯化钙 | 一氧化氮 | 氢氧化钠 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:X>Y>Z>W | |
| B. | Y的气态氢化物的热稳定性比W的强 | |
| C. | 原子半径的大小顺序:r(Z)>r(Y)>r(W)>r(X) | |
| D. | X分别与Y、Z形成的化合物中化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对稀土元素及化合物的研究是获得优良催化剂的一种重要途径 | |
| B. | 油脂是人体中热值最高的营养物质,在工业上可用于制肥皂和油漆 | |
| C. | 离子键、共价键和氢键等化学键都可能对物质的熔沸点产生影响 | |
| D. | 高分子膜在分离提纯、物质制备以及能量转化等领域都有广泛应用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 | |
| B. | NH3为三角锥形,甲烷是正四面体形 | |
| C. | NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较弱 | |
| D. | NH3和CH4都是sp3型杂化,键角都是109°28′ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | ① | ② | ③ | ④ |
| pH | 10 | 10 | 4 | 4 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
| A. | 相同体积③、④溶液分别与NaOH完全反应,消耗NaOH物质的量:③>④ | |
| B. | 分别加水稀释10倍,四种溶液的pH①>②>④>③ | |
| C. | ①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| D. | Va L ④溶液与Vb L ②溶液混合(近似认为混合溶液体积=Va+Vb),若混合后溶液pH=5,则Va :Vb=11:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
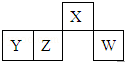 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A. | 原子半径:W>Z>Y>X | |
| B. | X的氢化物与氯化氢反应的产物溶于水形成的溶液呈酸性 | |
| C. | 最简单气态氢化物的热稳定性:Z>W | |
| D. | 含Y元素的盐溶液一定显酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com