
| A. | SO2具有还原性,可用于漂白纸浆 | |
| B. | 碱石灰具有吸水性,可用于干燥氯气 | |
| C. | 氢氟酸具有弱酸性,可用于蚀刻玻璃 | |
| D. | H2O2具有还原性,可用于与酸性高锰酸钾溶液反应制取少量氧气 |
分析 A.二氧化硫具有漂白性,能漂白纸张;
B.碱石灰具有碱性和吸水性,能和氯气反应;
C.HF能腐蚀玻璃;
D.双氧水具有氧化性和还原性,能被强氧化剂氧化.
解答 解:A.二氧化硫能和有色物质反应生成无色物质而具有漂白性,所以能漂白纸张,漂白纸张与二氧化硫的还原性无关,故A错误;
B.碱石灰具有碱性和吸水性,能和氯气反应,所以不能干燥氯气,故B错误;
C.HF属于弱酸,玻璃中含有二氧化硅,HF和二氧化硅反应生成四氟化硅和水,所以能腐蚀玻璃,故C错误;
D.双氧水具有氧化性和还原性,能被强氧化剂氧化,酸性高锰酸钾溶液呈强氧化性,能将双氧水氧化生成氧气,故D正确;
故选D.
点评 本题考查物质之间的反应,涉及气体的干燥、二氧化硫和HF的性质及氧化还原反应,明确反应原理是解本题关键,注意二氧化硫漂白性和还原性的区别,会根据气体性质选取合适的干燥剂,题目难度不大.


科目:高中化学 来源: 题型:解答题
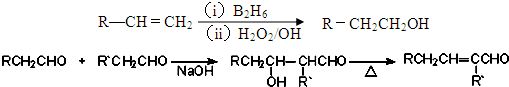
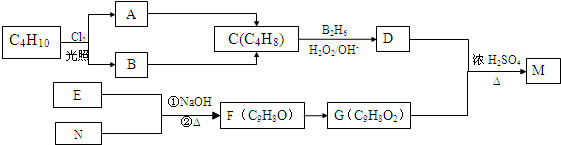
 、
、 ;
;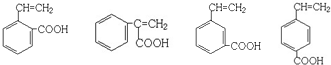 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 微粒半径:Cl->K+>Al3+>O2- | B. | 碱性:KOH>Ca(OH)2>Mg(OH)2 | ||
| C. | 晶体熔点:金刚石>氯化镁>汞>碘 | D. | 稳定性和还原性:H2O>H2S>AsH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 | |
| B. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| C. | 煎炸食物的花生油和牛油都是可皂化的饱和酯类 | |
| D. | 装饰材料释放的甲醛会造成污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | W分别与X、Y形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物的水化物的酸性比Z的弱 | |
| D. | Z的简单氢化物的热稳定性比W的强 |
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第三次月考模拟化学试卷 题型:选择题
硬脂酸甘油酯经皂化反应后,得到硬脂酸钠和甘油。欲分离出硬脂酸钠.应采用的方法是:①用滤纸过滤②用分液漏斗分液③加热蒸发④加入热的饱和食盐水
A.④③
B.④②
C.①③
D.④①
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )所示,回答下列问题.
)所示,回答下列问题.
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;取0.2mol/L的NaOH溶液与0.1mol/L的G溶液等体积混合后,加热至充分反应后,待恢复至室温,剩余溶液中离子浓度由大到小的顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+),此时测得溶液的pH=12,则此条件下G中阴离子的电离平衡常数Ka=4×10-12
;取0.2mol/L的NaOH溶液与0.1mol/L的G溶液等体积混合后,加热至充分反应后,待恢复至室温,剩余溶液中离子浓度由大到小的顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+),此时测得溶液的pH=12,则此条件下G中阴离子的电离平衡常数Ka=4×10-12查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com