

| A.加入NaOH溶液后过滤,滤渣为Fe(OH)3 |
| B.也可以先加硫酸,再加NaOH溶液后蒸发、冷却、结晶、过滤 |
| C.加硫酸后,溶液中的盐除含有硫酸铝外,还有硫酸钠 |
| D.如果滤渣2中含1molAl(OH)3,则至少需要1molNaOH才能使Al(OH)3完全溶解 |
科目:高中化学 来源:不详 题型:单选题
| A.BaCl2 | B.HCl | C.NaOH | D.Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中加入盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 该溶液中一定含有SO42— |
| B | 将少量的溴水滴入FeCl2、NaI的混合溶液中,再滴加CCl4,振荡、静置,向上层溶液中滴加KSCN溶液。再向上层溶液中滴加溴水 | 实验现象1: 上层溶液不变红, 下层溶液紫红色 实验现象2: 上层溶液变红 | 氧化性:Br2>Fe3+>I2 |
| C | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| D | BaSO4固体加入饱和Na2CO3溶液中,过滤,向滤渣中加入盐酸 | 有气体生成 | Ksp(BaCO3)<Ksp(BaSO4) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.萃取操作时,在选择萃取剂时,要求萃取剂和原溶剂不互溶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
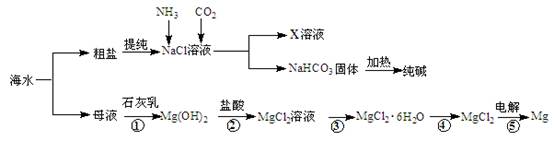
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.取少量待测溶液先加入BaCl2溶液,再加入足量的盐酸,有白色沉淀且不溶于盐酸,则该溶液中一定含有大量的SO42- |
| B.某无色溶液滴加氯水和CCl4,振荡、静置分层后,下层溶液显橙红色,则原溶液中有I- |
| C.用铂丝蘸取少量溶液进行焰色反应,火焰呈黄色,则该溶液一定是钠盐溶液 |
| D.取少量待测溶液滴加KSCN 溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Cr2O3)冶炼铬,简要流程如下:
Cr2O3)冶炼铬,简要流程如下:
 4Na2CrO4+Fe2O3+4CO2+______________。
4Na2CrO4+Fe2O3+4CO2+______________。
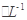 的硫酸亚铁铵[ (NH4)2Fe(SO4)
的硫酸亚铁铵[ (NH4)2Fe(SO4) ]滴定,终点时消耗b mL(此步骤的目的是用Fe2+把多余的Cr2O72-转化为)Cr3+。
]滴定,终点时消耗b mL(此步骤的目的是用Fe2+把多余的Cr2O72-转化为)Cr3+。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 CuY2–+ 2H+。则CuSO4·5H2O质量分数的表达式是 。
CuY2–+ 2H+。则CuSO4·5H2O质量分数的表达式是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
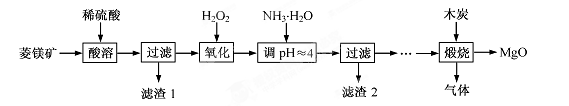
 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑ MgO+SO2↑+CO↑
MgO+SO2↑+CO↑ MgO+S↑+3CO↑
MgO+S↑+3CO↑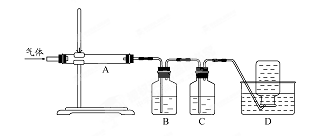
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com