
【题目】合金是建筑航空母舰的主体材料。
(1)航母升降机可由铝合金制造。
①铝元素在周期表中的位置是________________,工业炼铝的原料由铝土矿提取而得,提取过程中通入的气体为______________。
②Al—Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为____________________。焊接过程中使用的保护气为__________________(填化学式)。
(2)航母舰体材料为合金钢。
①舰体在海水中发生的电化学腐蚀主要为_______________腐蚀。
②航母用钢可由低硅生铁冶炼而成,则在炼铁过程中为降低硅含量需加入的物质为 。
(3)航母螺旋桨主要用铜合金制造。
①80.0 g Cu—Al合金用酸完全溶解后,加入过量氨水,过滤得到白色沉淀39.0 g,则合金中Cu的质量分数为___________________。
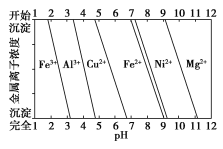
②为分析某铜合金的成分,用酸将其完全溶解后,用NaOH溶液调节pH,当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀。结合下图信息推断该合金中除铜外一定含有______________。
【答案】(1)①第三周期第ⅢA族 CO2
②Al2O3+2NaOH=2NaAlO2+H2O Ar(其他合理答案均可)
(2)①吸氧腐蚀 ②CaCO3或CaO (3)①83.1% ②Al、Ni
【解析】
试题分析:(1)①铝的原子序数是13,铝元素在周期表中的位置是第三周期第ⅢA族。铝土矿中的Al2O3与NaOH反应生成NaAlO2,通入CO2可生成氢氧化铝。
②Al2O3与NaOH反应生成NaAlO2和H2O,反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O;为防止合金被氧化,需要加惰性气体,如Ar等。
(2)①海水为中性,舰体中的钢发生吸氧腐蚀。②CaO能与生铁中的SiO2反应生成CaSiO3和CO2,从而降低生铁中硅的含量,因此在炼铁过程中为降低硅含量需加入的物质为氧化钙或碳酸钙。
(3)①白色沉淀为Al(OH)3,可得Cu的质量分数为:(80.0g-27 gmol1×39.0g/78 gmol1)/80.0g×100%=83.1%②根据题目所给图可以看出,Al3+在pH=3.4时开始转化为沉淀,说明合金中含Al,在pH为7.0、8.0时过滤沉淀,说明pH7.0到8.0范围内生成沉淀,根据图可以看出Ni2+在这个范围内转化为沉淀,说明合金中含Ni。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列物质的哪些用途与它的物理性质有关:①氩气和氮气作灯泡的保护气②用铝做炊具③用氧气作助燃剂④用碳作燃料⑤用花岗岩铺地面,以上说法正确的是( )
A.①②③④ B.①③⑤ C.②⑤ D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁在人体中的含量只有0.004%,微乎其微,但铁是组成血红蛋白的一个不可缺少的成员.正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁,服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收.
(1)在人体中进行Fe2+![]() Fe3+的转化时,①中的Fe2+作 剂;
Fe3+的转化时,①中的Fe2+作 剂;
(2)“服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话指出,维生素C在这一反应中作__________剂;
(3)用小苏打片(NaHCO3)治疗胃酸(主要成分盐酸)过多的离子方程式为 ;
如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质应用的说法正确的是( )
A.SO2具有漂白性,可用作熏蒸粉丝使其增白
B.常温下,二氧化硅不与强酸反应,可用石英容器盛放氢氟酸
C.铜的金属活泼性比铁的弱,可在铁船闸上装若干铜块以减缓其腐蚀
D.氧化铝熔点很高,可制造高温耐火材料,如制耐火管、坩埚等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是( )
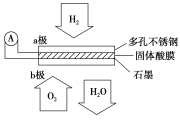
A.电子通过外电路从b极流向a极
B.H+由a极通过固体酸电解质传递到b极
C.b极上的电极反应式为:O2+2H2O+4e-=4OH-
D.每转移0.1 mol电子,消耗1.12 L的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其保持平衡,然后向左侧烧杯中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(不考虑两球的浮力变化)( )

A.杠杆为导体或绝缘体时,均为A端高B端低
B.杠杆为导体或绝缘体时,均为A端低B端高
C.当杠杆为导体时,A端高B端低
D.当杠杆为导体时,A端低B端高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸、硫酸和硝酸是常见的“三大酸”。现就三大酸与金属铜反应的情况,回答问题:
(1)稀盐酸不与Cu 反应,若在稀盐酸中加入H2O2后,则可使铜顺利溶解。该反应的化学方程式为:____________________________。
(2)在一定体积的10mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积__________(填“大于”、“ 等于”或“小于”)180mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为_____________________。
(3)镁铁混合物4.8g,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下2 .24LNO气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是_________克。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com