
| A£® | ÉĻŹö·“Ó¦ÖŠŃõ»Æ²śĪļÖ»ÓŠN2 | |
| B£® | µ±ÓŠ0.4molCO2Éś³ÉŹ±£¬·“Ó¦ÖŠ×ŖŅʵĵē×ÓµÄ×ÜŹżÄæŌ¼ĪŖ1.204”Į1024 | |
| C£® | ČōÉĻŹö·“Ӧɜ³É0.4molCO2£¬ŌņČÜŅŗÖŠŅõĄė×ÓŌö¼ÓµÄĪļÖŹµÄĮæĪŖ2mol | |
| D£® | ĻÖČ”1Lŗ¬CN-1.02mg/LµÄ·ĻĖ®£¬ÖĮÉŁŠčÓĆ4.0”Į10-5molCl2“¦Ąķŗó²Å·ūŗĻÅŷűź×¼ |
·ÖĪö ·“Ó¦2CN-+8OH-+5Cl2=2CO2”ü+N2”ü+10Cl-+4H2OÖŠ£¬ClŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ0½µµĶĪŖ-1¼Ū£¬NŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ-3¼ŪÉżøßĪŖ0£¬CŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+2¼ŪÉżøßĪŖ+4¼Ū£¬øĆ·“Ó¦ÖŠ×ŖŅĘ10e-£¬ŅŌ“Ė½ā“š£®
½ā“š ½ā£ŗA£®C”¢NŌŖĖŲ»ÆŗĻ¼Ū¶¼Éżøߣ¬ŌņŃõ»Æ²śĪļÓŠN2”¢CO2£¬¹ŹA“ķĪó£»
B”¢ÓÉ·“Ó¦æÉÖŖ£¬Éś³É2molCO2Ź±£¬×ŖŅĘ10molµē×Ó£¬ŌņÓŠ0.4 mol CO2Éś³ÉŹ±£¬·“Ó¦ÖŠ×ŖŅʵĵē×ÓµÄ×ÜŹżÄæŌ¼ĪŖ$\frac{0.4}{2}$mol”Į10”ĮNA=2”Į6.02”Į1023£¬¹ŹBÕżČ·£»
C”¢ÓÉ·“Ó¦æÉÖŖ£¬Éś³É2molCO2µÄĶ¬Ź±£¬Éś³É10molCl-£¬·“Ó¦Ē°ŗóŅõĄė×ÓŹżÄæ²»±ä£¬Ōņµ±ÓŠ0.2mol CO2Éś³ÉŹ±£¬ČÜŅŗÖŠŅõĄė×ÓµÄĪļÖŹµÄĮæ²»±ä£¬¹ŹC“ķĪó£»
D£®n£ØCN-£©=$\frac{1.02”Į1{0}^{-3}g}{26g/mol}$”Ö4.0”Į10-5mol£¬ÓÉ·½³ĢŹ½æÉÖŖŠčŅŖ1”Į10-4mol ĀČĘų£¬¹ŹD“ķĪó£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦µÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ·“Ó¦ÖŠŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»Æ¼°Ńõ»Æ»¹Ō·“Ó¦ÖŠ¹ęĀÉŠŌÖŖŹ¶ĪŖ½ā“šµÄ¹Ų¼ü£¬Ń”ĻīDĪŖ½ā“šµÄŅדķµć£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®
£® $\stackrel{Ņ»¶ØĢõ¼ž}{”ś}$
$\stackrel{Ņ»¶ØĢõ¼ž}{”ś}$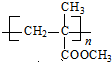 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
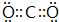 £®
£®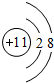 £¬D”¢E½įŗĻŠĪ³ÉµÄ»ÆŗĻĪļµÄµē×ÓŹ½
£¬D”¢E½įŗĻŠĪ³ÉµÄ»ÆŗĻĪļµÄµē×ÓŹ½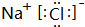 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢K+”¢$S{O_4}^{2-}$”¢$HC{O_3}^-$ | B£® | Cu2+”¢K+”¢$S{O_4}^{2-}$”¢$N{O_3}^-$ | ||
| C£® | Na+”¢K+”¢Cl-”¢$S{O_4}^{2-}$ | D£® | Fe2+”¢K+”¢$N{O_3}^-$”¢$C{H_3}CO{O^-}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ClO2ŹĒ»¹Ō²śĪļ | |
| B£® | H2C2O4ŌŚ·“Ó¦ÖŠ±»Ńõ»Æ | |
| C£® | 1molKClO3²Ī¼Ó·“Ó¦£¬×ŖŅʵē×ÓĪļÖŹµÄĮæĪŖ1mol | |
| D£® | Éś³É5.6LCO2£¬×ŖŅʵĵē×ÓŹżÄæĪŖ0.25NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “×ĖįČÜŅŗÓėNaOH·“Ó¦£ŗOH-+H+”śH2O | |
| B£® | ĻõĖįČÜŅŗŗĶĢ¼ĖįĒāÄĘ·“Ó¦£ŗH++2CO32-”śCO2”ü+H2O | |
| C£® | ½«äåĖ®¼ÓČėKIČÜŅŗÖŠ£ŗBr2+2I-”śI2+2Br- | |
| D£® | CO2ĶØČė³ĪĒåŹÆ»ŅĖ®£ŗ2OH-+CO2”śH2O+CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
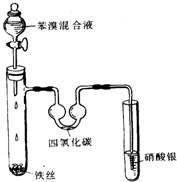 £Ø1£©±½·Ö×ÓÖŠµÄĢ¼Ģ¼Ö®¼äµÄ»Æѧ¼üŹĒŅ»ÖÖ¶ĄĢŲµÄ¼ü£¬Ņņ“ĖĘä»ÆѧŠŌÖŹŅ»°ć±ķĻÖ
£Ø1£©±½·Ö×ÓÖŠµÄĢ¼Ģ¼Ö®¼äµÄ»Æѧ¼üŹĒŅ»ÖÖ¶ĄĢŲµÄ¼ü£¬Ņņ“ĖĘä»ÆѧŠŌÖŹŅ»°ć±ķĻÖ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŃĪĖį | B£® | NH3 | C£® | ČŪČŚµÄK2O | D£® | BaSO4¾§Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | Ąė ×Ó | ŅŖ Ēó |
| A | K+”¢NO3-”¢Cl-”¢SO42- | c£ØK+£©£¼c£ØCl-£© |
| B | Ca2+”¢NO3-”¢CO32-”¢Cl- | ÖšµĪ¼ÓČėŃĪĖįĮ¢¼“ÓŠĘųĢå²śÉś |
| C | Na+”¢Cu2+”¢Mg2+”¢SO42- | ÖšµĪ¼ÓČėNaOHČÜŅŗĮ¢¼“ÓŠ³Įµķ²śÉś |
| D | H+”¢NH4+”¢Al3+”¢SO42- | ÖšµĪ¼ÓČėNaOHČÜŅŗĮ¢æĢÓŠĘųĢå²śÉś |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com