
 2Z���������ﵽƽ��ʱ��ƽ������Z���������Ϊ0.4���Իش������й����⣺
2Z���������ﵽƽ��ʱ��ƽ������Z���������Ϊ0.4���Իش������й����⣺ һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Z+W���������������������£�����ѹǿ����Ӧ���ʱ仯ͼ����ͼ��ʾ����ͼ���й���X��Y��Z��W�������ʵľۼ�״̬Ϊ
Z+W���������������������£�����ѹǿ����Ӧ���ʱ仯ͼ����ͼ��ʾ����ͼ���й���X��Y��Z��W�������ʵľۼ�״̬Ϊ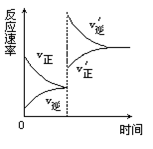
| A��Z��W��Ϊ���壬X��Y����һ�������� |
| B��Z��W����һ�������壬X��Y�Է����� |
| C��X��Y��Z��W�Է����� |
| D��X��Y��Ϊ���壬Z��W����һ��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C���ﵽƽ��ı�־��
2C���ﵽƽ��ı�־��| A��C������������B������������� | B��A��B��C��Ũ�Ȳ��ٷ����仯 |
| C��A��B��C�ķ�����֮��Ϊ1��3��2 | D����λʱ��������A n mol��ͬʱ����B 3n mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH(g)��H2O(g)+ 49kJ
CH3OH(g)��H2O(g)+ 49kJ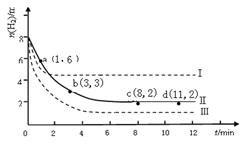
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2R(g)����H>0 ��y ���ʾ����
2R(g)����H>0 ��y ���ʾ����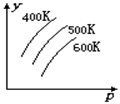
| A��ƽ��ʱ���������R�İٷֺ��� |
| B��ƽ��ʱ���������G�İٷֺ��� |
| C��G��ת���� |
| D��L��ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 ����4 s��ﵽƽ��״̬�����SO2�����ʵ�����3mol�����㣺��1����O2��ʾ�ĸ÷�Ӧ�����ʣ���2��ƽ��ʱSO3�����ʵ���Ũ�ȡ�
����4 s��ﵽƽ��״̬�����SO2�����ʵ�����3mol�����㣺��1����O2��ʾ�ĸ÷�Ӧ�����ʣ���2��ƽ��ʱSO3�����ʵ���Ũ�ȡ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
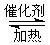 2SO3(g)����H<0��ij�¶��£���2 mol SO2��
2SO3(g)����H<0��ij�¶��£���2 mol SO2�� 1 mol O2����10 L�ܱ������У���Ӧ��ƽ���
1 mol O2����10 L�ܱ������У���Ӧ��ƽ��� ��SO2��ƽ��ת����(��)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ����ʾ��������˵����ȷ����
��SO2��ƽ��ת����(��)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ����ʾ��������˵����ȷ����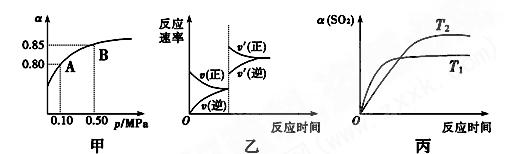
| A����ͼ��֪��A��SO2��ƽ��Ũ��Ϊ0.4 mol��L��1 |
| B����ͼ��֪��B��SO2��O2��SO3��ƽ��Ũ��֮��Ϊ2��1��2 |
| C����ƽ�����С�����ݻ�����Ӧ���ʱ仯ͼ�������ͼ�ұ�ʾ |
D��ѹǿΪ0.50 MPaʱ��ͬ�¶��� SO2ת�������¶ȹ�ϵ���ͼ����T2>T1 SO2ת�������¶ȹ�ϵ���ͼ����T2>T1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
 ��
�� )��c(H2)=c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ_____________
)��c(H2)=c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ_____________�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 W+Z����Ӧ���ʣ�V����ʱ�䣨t���仯�������ͼ��ʾ��
W+Z����Ӧ���ʣ�V����ʱ�䣨t���仯�������ͼ��ʾ��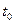 ��ʾ�������������������£��ı���ϵ��һ���������¶ȡ�Ũ�ȡ�ѹǿ��������ı仯�������з�����ȷ����
��ʾ�������������������£��ı���ϵ��һ���������¶ȡ�Ũ�ȡ�ѹǿ��������ı仯�������з�����ȷ����
A�� ʱ�����ı�����ı仯��ƽ��������Ӧ�����ƶ� ʱ�����ı�����ı仯��ƽ��������Ӧ�����ƶ� |
B���� �ı� �ı� ��������ѹǿ����W��Z��Ϊ���壬X��Y��ֻ��һ��Ϊ���� ��������ѹǿ����W��Z��Ϊ���壬X��Y��ֻ��һ��Ϊ���� |
C����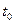 �ı���������� �ı���������� �ȣ���÷�Ӧ������Ӧ�����ȷ�Ӧ �ȣ���÷�Ӧ������Ӧ�����ȷ�Ӧ |
D����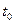 �ı��������Ũ�ȣ��ı�ķ����Ǽ�СX��Y��Ũ�� �ı��������Ũ�ȣ��ı�ķ����Ǽ�СX��Y��Ũ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com