
| A. | 0.1 mol•L-1 | B. | 1.0 mol•L-1 | C. | 0.3 mol•L-1 | D. | 0.4 mol•L-1 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
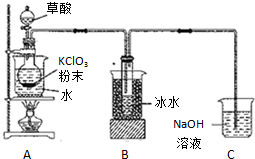 二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用KClO3粉末与草酸(H2C2O4)在60℃时反应可生成ClO2等物质,实验装置如图所示:
二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用KClO3粉末与草酸(H2C2O4)在60℃时反应可生成ClO2等物质,实验装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
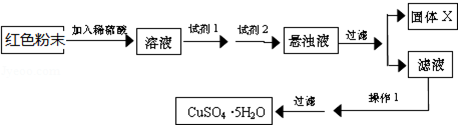
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
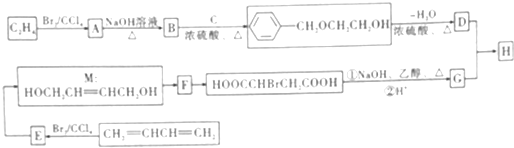
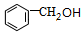 ,F中官能团的名称为羟基、溴原子
,F中官能团的名称为羟基、溴原子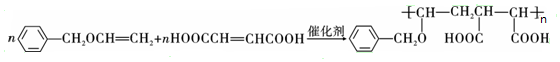
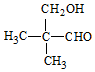 或
或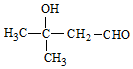 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
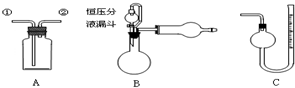
| A. | 装置A从①进气,用排水法可收集NO气体 | |
| B. | 装置A中盛饱和Na2CO3溶液,从①进气除去CO2中混有的HCl | |
| C. | 装置A、B组合,从A中①进气可制备、收集干燥纯净的NH3 | |
| D. | 装置B、C组合,可测定一定质量样品中Zn的氧化程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 此时溶液可能为中性 | |
| B. | 此时溶液中NH4+的浓度一定增大 | |
| C. | 此时NH4+的水解程度一定增大 | |
| D. | 此过程中,溶液中NH3•H2O和NH4+的数目之和一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +283.5 kJ•mol-1 | B. | -172.5 kJ•mol-1 | C. | +172.5 kJ•mol-1 | D. | -504 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com