

| △c |
| △t |
| 0.2mol/L |
| 10min |
| 1.0-0.8 |
| 1.0 |
| 0.8-0.4 |
| 0.8 |
| 0.4-0.3 |
| 0.4 |
| c2(CO2)?c(N2) |
| c2(NO2) |
| 0.62×0.3 |
| 0.42 |


 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:
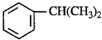
查看答案和解析>>
科目:高中化学 来源: 题型:
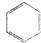 看,分子中含有碳碳双键,由此推测,苯能使酸性高锰酸钾溶液褪色且苯的6个碳原子之间的键有两种.
看,分子中含有碳碳双键,由此推测,苯能使酸性高锰酸钾溶液褪色且苯的6个碳原子之间的键有两种.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 Ⅰ、碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)?WI2(g).
Ⅰ、碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)?WI2(g).查看答案和解析>>
科目:高中化学 来源: 题型:
 ,俗名为水杨酸,在 医学上具有解热镇痛和抗炎、抗风湿作用,由于它具有酸性而刺激胃肠道产生严重的反应,因此通常将它先转化为乙酰水杨酸(阿司匹林),服用后在人体内会缓慢反应生成水杨酸:
,俗名为水杨酸,在 医学上具有解热镇痛和抗炎、抗风湿作用,由于它具有酸性而刺激胃肠道产生严重的反应,因此通常将它先转化为乙酰水杨酸(阿司匹林),服用后在人体内会缓慢反应生成水杨酸:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-=Cl2↑+Mn2++H2O |
| B、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| C、2mol氢气和1 mol氧气化合生成2 mol液态水,放出571.6kJ热量的热化学方程式2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ?mol-1 |
| D、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com