
| A. | 常温下,Cl2与NaOH溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 稀H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H+十SO42-═BaSO4↓+H2O | |
| D. | 氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- |
分析 A.氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
B.小苏打为碳酸氢钠,碳酸氢钠少量,反应生成碳酸钙沉淀、氢氧化钠和水;
C.氢离子、氢氧根离子的系数与硫酸、氢氧化钡的化学式不相符;
D.氯化亚铁被氯气 氧化成氯化铁.
解答 解:A.常温下Cl2与NaOH溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故A正确;
B.澄清石灰水与少量小苏打溶液混合,反应生成碳酸钙沉淀、氢氧化钠和水,反应的离子方程式为:Ca2++OH-+HCO3-═CaCO3↓+H2O,故B正确;
C.稀H2SO4与Ba(OH)2溶液反应生成硫酸钡沉淀和水,正确的离子方程式为:Ba2++2OH-+2H+十SO42-═BaSO4↓+2H2O,故C错误;
D.氯化亚铁溶液中通入氯气,反应生成氯化铁,该离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,故D正确;
故选C.
点评 本题考查了离子方程式的书写方法,为高考的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等;试题有利于培养学生的分析能力及灵活应用能力.


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 碱性氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH- | |
| B. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ | |
| C. | 用惰性电极分别电解熔融氯化钠和饱和食盐水时,阳极的电极反应式均为:2Cl--2e-=Cl2↑ | |
| D. | 钢铁发生吸氧腐蚀时的正极反应式:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | RCOOH与R′OH发生酯化反应时生成R′OOCR | |
| B. | 能与NaOH溶液反应,分子式为C2H4O2的有机物一定是羧酸 | |
| C. | 甲酸乙酯、乙酸甲酯、丙酸互为同分异构体 | |
| D. | 甲醛与乙酸乙酯的最简式相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氧化还原反应中,还原剂一定是失去电子的反应物 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 某元素从化合态转变为游离态时,该元素一定被还原 | |
| D. | 金属阳离子被还原不一定得到金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
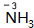 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com