
| ʵ���� | ʵ��Ŀ�� | t�� | ���� | Ũ�� |
| ����ʵ��� | ��ʵ����� | 25 | 3��FeCl3��Һ | 10ml 2%H2O2 |
| ����ʵ��� | ̽��Ũ�ȶ����ʵ�Ӱ�� | 25 | 10ml 5%H2O2 |
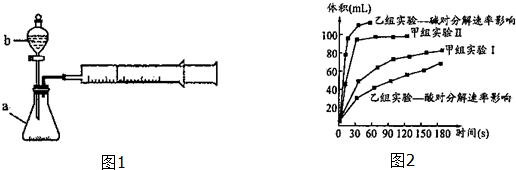
���� ��1����ͼ��֪����b�Ƿ�Һ©����
��2������ʵ�����̽��Ũ�ȶ����ʵ�Ӱ�죬��������Ҫ��ȫ��ͬ��������
��3���������-ʱ��ͼ�У�б�ʼ��ɴ�����ѧ��Ӧ���ʣ�
���������о����ᡢ���H2O2�ֽ�Ӱ�����ص����ݷ�����֪����Խǿ����ͼ��֪����ǿ�ֽ�����Խ�죻
��������֪Ba02������H2SO4��Һ��Ӧ��H202�ķ�Ӧ��ΪBa02��H2SO4������ΪH202������ԭ���غ��֪��һ�ֲ���Ϊ���ᱵ����ͼ��֪���������£�H202�ֽ����������
��� �⣺��1����ͼ��֪����b�Ƿ�Һ©����
�ʴ�Ϊ����Һ©����
��2������ʵ����ʵ��Ŀ��Ϊ̽��Ũ�ȶ����ʵ�Ӱ�죬����ʵ���ʵ��Ŀ�Ŀ�֪������Ũ��ֻ����һ����Ϊ��������Ũ����Ϊ�����������Ͳ�������Ϊ���������Լ���ʵ����д��������ʵ����е���ͬ��
�ʴ�Ϊ��
| ʵ���� | ʵ��Ŀ�� | t�� | ���� | Ũ�� |
| ����ʵ��� | 3��FeCl3��Һ |
���� ���⿼��������ضԻ�ѧ��Ӧ���ʵ�Ӱ�죬ע����Ʊ������������ۺ��Խ�ǿ���Ѷ����У�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ͳ�Ʒ����������о���ʵ�鷽����ģ�ͻ��������ǻ�ѧ�о��ij��÷��� | |
| B�� | ����������������ֹ����ȡ��������ͭ��ú��������ȡ���ȹ��̶��漰��ѧ�仯 | |
| C�� | ��2016��1��1�ſ�ʼ�㽭ʡ���ͱ��ɡ���������ߵ�����V�������Ⲣ����ζ�����������ŷŵ������� | |
| D�� | ��������������Ƽ����ķ�չ����ʹ���Ӿ���ܡ�����оƬ�����ӵ��ߡ����Ӽ�����Ȼ�ѧ�����õ��㷺��Ӧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
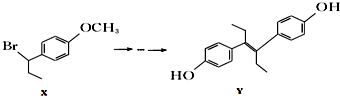
| A�� | ������x�в���������̼ԭ�� | |
| B�� | 1mol������Y��Ũ��ˮ��Ӧ���������5mol Br2 | |
| C�� | ��һ�������»�����Y�ܷ����Ӿ۷�Ӧ�����۷�Ӧ | |
| D�� | ����������ˮ��Һ�м��ȣ�������X�ܷ�����ȥ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼ԭ�Ӽ䶼�Ե������������������� | |
| B�� | �����������ʶ�����ζ | |
| C�� | ����֬�������ڸ����� | |
| D�� | ����������ǻ�Ϊͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
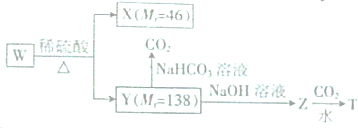
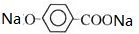 +CO2+H2O��
+CO2+H2O��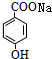 +NaHCO3��
+NaHCO3��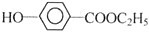
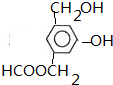 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ���� | �� | �� | �� | �� | �� |
| c��I-��/mol/L | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c��S2O${\;}_{8}^{2-}$��/mol/L | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
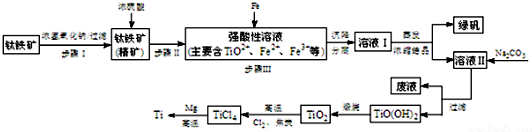
| pH | Fe��OH��3 | Fe��OH��2 | Mg��OH��2 | Ti��OH��2 |
| ��ʼ���� | 1.1 | 4.5 | 7 | 1 |
| ��ȫ���� | 2.8 | 6.4 | 9.2 | 2.7 |
| TiCl4 | Mg | MgCl2 | Ti | |
| �۵�/�� | -25.0 | 648.8 | 714 | 1667 |
| �е�/�� | 136.4 | 1090 | 1412 | 3287 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
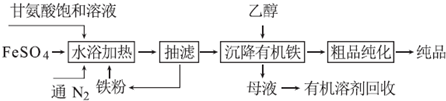
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
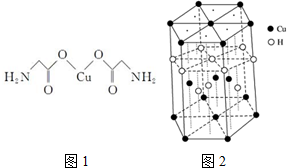
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com