
分析 A、B、C、D是周期表中前10号元素,它们的原子半径依次减小;D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取sp3杂化,则D是H元素、A是C、B是N、C是O元素,M、N、W分别是CH4、NH3、H2O,
①同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第IVA族元素第一电离能大于其相邻元素;
②M是CH4,为正四面体结构,不同非金属元素之间存在极性键,正负电荷重心不重合的分子为极性分子;
③氢键影响物质熔沸点;
④W是H2O,H2O分子中O原子价层电子对个数是4且含2个孤电子对,根据价层电子对互斥理论判断其VSEPR模型和空间构型;
⑤CN-离子与N2互为等电子体,二者结构相似,故其电子式为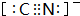 ,根据二者结构确定π键数目之比.
,根据二者结构确定π键数目之比.
解答 解:A、B、C、D是周期表中前10号元素,它们的原子半径依次减小;D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取sp3杂化,则D是H元素、A是C、B是N、C是O元素,M、N、W分别是CH4、NH3、H2O,
①同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第IVA族元素第一电离能大于其相邻元素,N元素位于第VA族,所以A、B、C第一电离能大小顺序是N>O>C,
故答案为:N>O>C;
②M是CH4,为正四面体结构,甲烷分子中C-H原子之间存在极性键,甲烷分子正负电荷重心重合,为非极性分子,故答案为:极性;非极性;
③N为NH3,因为氨分子间存在氢键,分子间作用力大,因而易液化,
故答案为:氨分子间存在氢键,分子间作用力大,因而易液化;
④W是H2O,H2O分子中O原子价层电子对个数是4且含2个孤电子对,根据价层电子对互斥理论判断其VSEPR模型为正四面体结构、空间构型为V形,故答案为:正四面体;V形;
⑤CN-离子与N2互为等电子体,二者结构相似,故其电子式为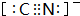 ,AB-离子中和B2分子的π键数目比=2:2=1:1,故答案为:1:1.
,AB-离子中和B2分子的π键数目比=2:2=1:1,故答案为:1:1.
点评 本题考查位置结构性质相互关系及应用,涉及化学键、分子空间构型判断、氢键等知识点,侧重考查学生分析判断能力,明确原子结构、元素周期表结构、物质结构等是解本题关键,注意第一电离能大小规律及异常现象,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
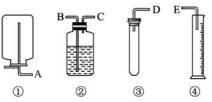 现有如下药品和装置:质量为w(w<1g)的锌片、稀H2SO4、无水硫酸铜和蒸馏水,设计一个简单实验,测定Zn的相对原子质量(气体体积均可认为是在标准状况下测定)如图
现有如下药品和装置:质量为w(w<1g)的锌片、稀H2SO4、无水硫酸铜和蒸馏水,设计一个简单实验,测定Zn的相对原子质量(气体体积均可认为是在标准状况下测定)如图查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀 | |
| B. | 水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染 | |
| C. | 清晨,在茂密的树林中,常常可以看到枝叶间透过的一道道光线 | |
| D. | 肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com