
| A. | 1mol 最多能与8molNaOH发生反应 最多能与8molNaOH发生反应 | |
| B. | 甲苯既能跟溴水反应又能跟酸性高锰酸钾溶液反应 | |
| C. | 向苯酚钠溶液中通入少量的CO2气体,发生反应的离子方程式为: 2 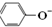 +H2O+CO2→2 +H2O+CO2→2 +CO${\;}_{3}^{2-}$ +CO${\;}_{3}^{2-}$ | |
| D. | 1mol 最多能和4molH2发生反应 最多能和4molH2发生反应 |
分析 A.有机物含有6个酚羟基和1个酯基,都可与氢氧化钠溶液反应;
B.甲苯与溴水不反应;
C.向苯酚钠溶液中通入少量的CO2气体生成碳酸氢钠;
D. 中苯环、碳碳双键和醛基都可与氢气发生加成反应.
中苯环、碳碳双键和醛基都可与氢气发生加成反应.
解答 解:A.有机物含有6个酚羟基和1个酯基,都可与氢氧化钠溶液反应,且酯基水解生成羧基和酚羟基,则1mol 最多能与8molNaOH发生反应,故A正确;
最多能与8molNaOH发生反应,故A正确;
B.甲苯与溴水不反应,与高锰酸钾可发生氧化还原反应,故B错误;
C.向苯酚钠溶液中通入少量的CO2气体生成碳酸氢钠,离子方程式为 +CO2+H2O→
+CO2+H2O→ +HCO3-,故C错误;
+HCO3-,故C错误;
D. 中苯环、碳碳双键和醛基都可与氢气发生加成反应,则1mol
中苯环、碳碳双键和醛基都可与氢气发生加成反应,则1mol 最多能和5molH2发生反应,故D错误.
最多能和5molH2发生反应,故D错误.
故选A.
点评 本题考查有机物的结构与性质,侧重有机物性质的考查,为高频考点,注意把握有机物的结构和官能团的性质,为解答该类题目的关键,难度不大.


科目:高中化学 来源: 题型:解答题
| T(℃) | 700 | 800 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 盐泥是氯碱工业中的废渣,主要含有镁、铁、铝、钙等的硅酸盐和碳酸盐.实验室以盐泥为原料制取MgSO4•7H2O的流程如下:[29g盐泥]$→_{②H_{2}SO_{4}调pH=1-2}^{①水,调成泥浆}$$→_{④过滤}^{③煮沸}$[滤液Ⅰ]$→_{⑥煮沸,趁热}^{⑤加NaClO,pH=5~6}$[滤液Ⅱ]→产品
盐泥是氯碱工业中的废渣,主要含有镁、铁、铝、钙等的硅酸盐和碳酸盐.实验室以盐泥为原料制取MgSO4•7H2O的流程如下:[29g盐泥]$→_{②H_{2}SO_{4}调pH=1-2}^{①水,调成泥浆}$$→_{④过滤}^{③煮沸}$[滤液Ⅰ]$→_{⑥煮沸,趁热}^{⑤加NaClO,pH=5~6}$[滤液Ⅱ]→产品查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol氢气所占体积约为22.4 L | |
| B. | 气态物质所占的体积主要由分子数目和分子间距离决定的 | |
| C. | 1 mol O2与1 mol O3所含的分子数目相等 | |
| D. | 物质的聚集状态不同主要是构成物质的基本粒子间的距离不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com