
| A. | 在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多 | |
| B. | 同价态的阳离子,甲比乙的氧化性弱 | |
| C. | 甲不能跟稀盐酸反应放出氢气而乙能 | |
| D. | 将甲、乙作电极组成原电池时,甲是正极 |
分析 金属的金属性越强,其最高价氧化物的水化物碱性越强,金属单质的还原性越强,其单质与水或酸反应越剧烈,据此分析解答.
解答 解:A.金属的金属性强弱与失电子多少无关,如等物质的量的Al、Mg分别和足量稀盐酸反应,铝失电子多,但金属性Mg>Al,故A错误;
B.金属的金属性越强,阳离子氧化性越弱,甲比乙的氧化性弱,则金属性甲>乙,故B正确;
C.甲不能跟稀盐酸反应放出氢气而乙能,则金属性甲<乙,故C错误;
D.一般来说,原电池中较活泼金属作负极、较不活泼金属作正极,将甲、乙作电极组成原电池时,甲为正极,则金属性甲<乙,故D错误;
故选B.
点评 本题考查金属性强弱判断,为高频考点,明确金属性强弱判断方法是解本题关键,注意金属的金属性强弱与失电子难易程度有关,与失电子多少无关,易错选项是A.


科目:高中化学 来源: 题型:解答题
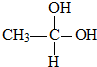 →CH3-CHO+H2O
→CH3-CHO+H2O
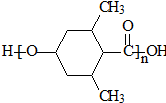 ]
]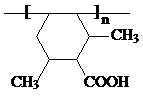 ;
;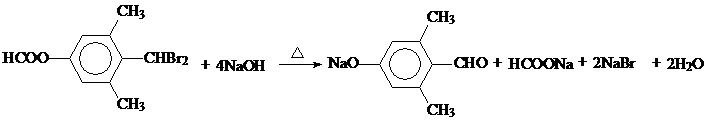 ;
;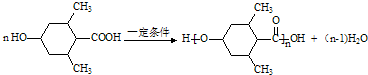 ;
;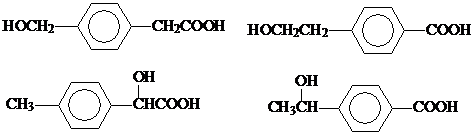 (任写一个).
(任写一个).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 宇宙原子总数的88.6%是氢 | B. | 地球上的元素绝大多数是金属 | ||
| C. | 普鲁特“氢是元素之母”的预言 | D. | 宇宙中存在少量稀有气体分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8gNa2O2中含有的阴离子数目为0.2Na | |
| B. | 标准状况下,2.24LCHCl3的分子数为0.1NA | |
| C. | 0.1molFe与足量稀HNO3反应,转移电子数为0.3NA | |
| D. | 1L 0.1mol/L Al2(SO4)3溶液中,Al3+的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对应的最简单氢化物的热稳定性:Z>Y | |
| B. | X、Z、W三种元素形成的化合物既含离子键,又含共价键 | |
| C. | 元素X与Y形成的化合物中,每个原子都达到了8电子稳定结构 | |
| D. | X与Z可形成既含极性共价键又含非极性共价键的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌片插入硝酸银溶液中:Zn+Ag+=Zn2++Ag | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| C. | 稀硝酸和过量的铁粉:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O | |
| D. | 少量SO2气体通入NaOH溶液中:SO2+OH-=HSO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com