
【题目】 下列溶液中,Na+的物质的量浓度最大的是( )
A.1 mL 0.5 mol·L-1的NaNO3溶液B.100 mL 0.01 mol·L-1的NaCl溶液
C.100 mL 0.1 mol·L-1的NaOH溶液D.10 mL 0.1 mol·L-1的Na2SO4溶液
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是( )
A.乙烯具有可燃性,可用作果实的催熟剂
B.浓硫酸具有脱水性,可用于干燥CO2
C.氧化铝熔点很高,可用作耐高温材料
D.二氧化硫具有氧化性,可用于纸张漂白
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.键能越大,表示该分子越容易受热分解
B.共价键都具有方向性
C.在分子中,两个成键的原子间的距离叫键长
D.H—Cl的键能为431.8kJ·mol-1 , H—Br的键能为366kJ·mol-1 , 说明HCl比HBr分子稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据氢原子和氟原子的核外电子排布,对F2和HF分子中形成的共价键描述正确的是( )
A.两者都为s-sσ键
B.两者都为p-pσ键
C.前者为p-pσ键,后者为s-pσ键
D.前者为s-sσ键,后者为s-pσ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素周期表的说法正确的是
A.元素周期表有8个主族
B.0族原子的最外层电子数均为8
C.ⅠA族的元素全是金属元素
D.短周期是指第1、2、3周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,10L密闭容器中加入5mol SO2、4mol O2 , 经10min后反应达平衡时有3mol SO2发生了反应.试计算:
(1)用SO2表示该反应的反应速率为多少?
(2)O2的转化率为多少?
(3)平衡常数K为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸H2C2O4是二元弱酸.室温下向10mL 0.01molL﹣1 H2C2O4溶液中逐滴加入0.01molL﹣1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( ) 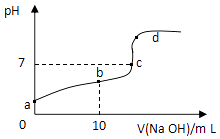
A.a点pH>2
B.b点表示的溶液中c(C2O42﹣)>c(H2C2O4)
C.c点时加入NaOH溶液的体积为20mL
D.d点存在c(Na+)+c(H+)=c(OH﹣)+2c(C2O42﹣)+c(HC2O4﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com