
| A. | 每一个反应,在一个温度下,有一个K值 | |
| B. | K越大,表示正向反应的倾向大,反应完全 | |
| C. | K值只能说明反应的最大限度,不能说明反应的速度 | |
| D. | 吸热反应的K值大于所有放热反应的K值 |
分析 A.对于确定的化学平衡,一定温度下反应的平衡常数一定;
B.平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,K越大说明正反应进行程度越大;
C.K是衡量化学平衡减小程度大小,和反应速率无关;
D.吸热反应不一定进行程度小,放热反应不一定进行程度大;
解答 姐:A.一定温度下的化学平衡,对应一个化学平衡常数,故A正确;
B.平衡常数是衡量化学平衡进行程度的物理量,K越大,表示正向反应的倾向大,反应越完全,故B正确;
C.平衡常数数值的大小是反应进行程度的标志,因为平衡状态是反应进行的最大限度,而平衡常数的表达式很好的表示出了在反应达到平衡时的生成物和反应物的浓度关系,一个反应的平衡常数越大,说明反应物的平衡转化率越高,和反应速率无直接关系,故C正确;
D.盐类水解是吸热反应,但平衡常数很小,吸热反应的K值不一定大于放热反应的K值,故D错误;
故选D.
点评 本题考查了化学平衡、化学平衡常数及其化学反应速率影响因素的分析,主要是平衡常数表达意义的理解应用,题目难度中等.


科目:高中化学 来源: 题型:解答题
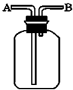 现有六种气体:H2、O2、NH3、SO2、NO2、NO.可以利用如图所示装置进行收集.
现有六种气体:H2、O2、NH3、SO2、NO2、NO.可以利用如图所示装置进行收集.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
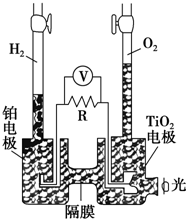 TiO2在光照射下可使水分解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图,电解质溶液为稀硫酸.下列叙述正确的是( )
TiO2在光照射下可使水分解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图,电解质溶液为稀硫酸.下列叙述正确的是( )| A. | 该装置只能将光能转化为电能 | |
| B. | TiO2电极上发生的反应为:2H++2e-═H2↑ | |
| C. | 该装置工作时,电流由TiO2电极经R流向铂电极 | |
| D. | 该装置工作时,TiO2电极附近溶液的pH变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
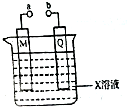
| A. | 若X、M、Q分别是H2SO4、Pb和PbO2,a、b连接后两极都有PbSO4生成 | |
| B. | 若X、M、Q分别是滴加酚酞的Na2SO4、C和Fe,a、b分别连接电源的正、负极,则通电后Q周围溶液颜色变红 | |
| C. | 若X、M、Q分别CuSO4、Cu和Fe,a、b分别连接电源的正、,则可在铁上镀铜 | |
| D. | 若X、M、Q分别是NaCl、C和Fe,则a、b连接后,M电极上有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LKOH溶液.整个实验过程溶液中c(OH-)的变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LKOH溶液.整个实验过程溶液中c(OH-)的变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是( )| A. | a点对应溶液中含有的分子有H2O、HClO、HCl、Cl2 | |
| B. | b点对应溶液中:c(H+)>c(Cl-)>c(HClO)>c(ClO-)>c(OH-) | |
| C. | c点对应溶液中:c(K+)=c(Cl-)+c(ClO-)+c(HClO) | |
| D. | 实验过程中可以用pH试纸测定溶液的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2SO4 | B. | H2SO4 | C. | Ba(OH)2 | D. | AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H3PW12O40在该酯化反应中起催化作用 | |
| B. | 杂多酸盐Na2HPW12O40与Na3PW12O40都是强电解质 | |
| C. | H3PW12O40、KH2PW12O40与Na3PW12O40中含有的原子团不同 | |
| D. | 硅钨酸H4SiW12O40也是一种杂多酸,其中W的化合价为+6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com