
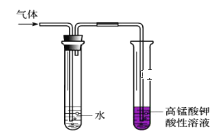
【题目】(1)实验室用酸性高锰酸钾检验溴乙烷与NaOH乙醇溶液反应生成的乙烯气体,如图,在通入酸性高锰酸钾之前为什么要先通入水中:_______;也可以用______代替酸性高锰酸钾,此时________(填“有必要”“没必要”)将气体通入水中。
(2)实验室用饱和食盐水与电石反应制取乙炔气体,发生反应的化学方程式为________,产生的气体含有H2S等杂质,用硫酸铜溶液除去,写出除H2S的离子反应方程式______。
(3)写出中子数为2的一种氦的核素_________。
(4)对苯二酚与浓溴水充分反应,消耗两者的物质的量之比为______。
【答案】除去挥发出来的乙醇,乙醇也能使酸性高锰酸钾褪色,避免造成干扰 溴水 没必要 CaC2+2H2O→Ca(OH)2+C2H2↑ H2S+Cu2+=CuS↓+2H+ ![]() 1:4
1:4
【解析】
(1)因为乙醇也能使高锰酸钾溶液褪色,所以通入水中吸收会发出来的乙醇,防止对实验造成干扰;如果用溴水的话也可以检验乙烯,同时乙醇不能使溴水褪色,所以没有必要先通入水中,来除去挥发出来的乙醇;
(2)电石和水剧烈反应生成乙炔,饱和食盐水是用来降低化学反应速率的,反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑,电石中往往含有P和S的杂质,生成的H2S气体可以被CuSO4溶液或CuCl2溶液吸收,生成难溶的CuS沉淀,离子方程式为:H2S+Cu2+=CuS↓+2H+;
(3)氦的质子数为2,中子数为2的话,那么质量数为4,所以满足要求的氦的核素为![]() ;
;
(4)酚羟基和溴水发生取代反应,只取代邻位和对位的氢原子,根据对苯二酚的结构,判断出对位有酚羟基,所以分别取代羟基邻位的氢原子,所以消耗两者的物质的量之比为1:4。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 | H2C2O4 | K1=5.4×10-2 | H2S | K1=1.3×10-7 |
HClO | 3×10-8 | K2=4.7×10-11 | K2=5.4×10-5 | K2=7.1×10-15 |
请回答下列问题:
(1) 同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是_________。
(2) 0.1mo1/L的H2C2O4溶液与0.1mo1/L的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为________________。
(3)pH相同的NaC1O和CH3COOK溶液中,[c(Na+)-c(C1O-)]______[c(K+)-c(CH3COO-)](填“>”、“<”或“=”) 。
(4) 向0.1mo1/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH): c(CH3COO-)=5:9,此时溶液pH=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,对下列叙述的判断正确的是
A. 物质的量浓度c (甲)>10c(乙)
B. 甲中水电离出来的H+的物质的量浓度是乙中水电离出来的H+的物质的量浓度的10倍
C. 中和等物质的量的NaOH溶液需甲、乙两杯醋酸溶液的体积,V(甲)=10V(乙)
D. 甲中的c (OH-)为乙中的c (OH-)的10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属加工前常用盐酸对金属表面氧化物进行清洗,会产生酸洗废水。pH在2左右的某酸性废水含铁元素质量分数约3%,其他金属元素如铜、镍、锌浓度较低,综合利用酸洗废水可制备三氯化铁。制备过程如下:
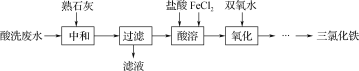
相关金属离子生成氢氧化物沉淀的pH如下表:
Fe(OH)3 | Cu(OH)2 | Ni(OH)2 | Zn(OH)2 | |
开始沉淀的pH | 1.5 | 4.2 | 7.1 | 5.4 |
沉淀完全的pH | 3.7 | 6.7 | 9.2 | 8.0 |
回答下列问题:
(1)“中和”时调节pH至________,有利于后续制备得纯度较高的产品。
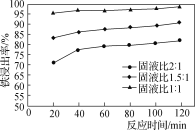
(2)处理酸洗废水中和后的滤渣,使铁元素浸出。按照不同的固液比投入“过滤”后滤渣和工业盐酸进行反应的铁浸出率如图所示,实际生产中固液比选择1.5∶1的原因是__________________。
(3)写出“氧化”中发生反应的离子方程式:____________________________________。
(4)“酸溶”后需根据溶液中Fe2+含量确定氧化剂的投入量。用K2Cr2O7标准溶液测定Fe2+(Cr2O![]() 被还原为Cr3+)的含量,该反应离子方程式为____________________________。
被还原为Cr3+)的含量,该反应离子方程式为____________________________。
(5) 将三氯化铁溶液在一定条件下________、________、过滤、洗涤、在氯化氢气氛中干燥得FeCl3·6H2O晶体,在实验室过滤装置中洗涤固体的方法是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
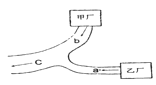
【题目】甲、乙两个化工厂分布在如图所示位置,箭头所指为工厂排水渠中水流方向。如果a处取得的水样经验测只含少量硝酸和硝酸钡,在c入取得的水样经检测pH=7,且只含少量硝酸钠,则b处的水中含有的物质应是下列物质中的
A. MgSO4、NaCl
B. K2SO4、NaOH
C. KOH、Na2SO4
D. NaOH、Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ,某有机物分解的反应可表示为:
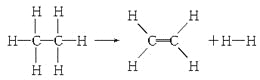
若在反应中消耗了1 mol乙烷(反应物),则有关该反应的说法正确的是( )
A. 该反应放出251.2 kJ的热量 B. 该反应吸收251.2 kJ的热量
C. 该反应放出125.6 kJ的热量 D. 该反应吸收125.6 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是
A. 合成氨工厂选择500℃的高温
B. 常温时,AgCl 在饱和氯化钠溶液中的溶解度小于在水中的溶解度
C. 热的纯碱溶液去油污效果更好
D. 开启啤酒瓶后,瓶中马上泛起大量泡沫
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com