
甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油。
已知:①CH4 (g) + H2O (g)= CO (g)+3H2 (g) △H1=+206.2kJ·mol-1
② CH4(g)+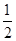 O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
③CH4 (g) + 2H2O (g) =CO2 (g) +4H2 (g) △H3="+165.0" kJ·mol-1
(1)CH4(g)与CO2 (g)反应生成CO(g)和H2(g)的热化学方程式为 。
(2)从原料选择和能源利用角度,比较方法①和②,为合成甲醇,用甲烷制合成气的适宜方法为 (填序号),其原因是 。
(3)合成气中的H2可用于生产NH3,在进入合成塔前常用Cu(NH3)2Ac溶液来吸收其中的CO,防止合成塔中的催化剂中毒,其反应是:
Cu(NH3)2Ac + CO + NH3 [Cu(NH3)3]Ac·CO △H<0
[Cu(NH3)3]Ac·CO △H<0
Cu(NH3)2Ac溶液吸收CO的适宜生产条件应是 。
(4)将CH4设计成燃料电池,其利用率更高,装置示意如右图(A、B为多孔性碳棒)。持续通入甲烷,在标准状况下,消耗甲烷体积VL。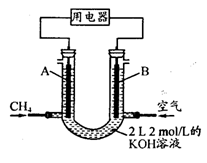
① 0<V≤44.8 L时,电池总反应方程式为 ;
② 44.8 L<V≤89.6 L时,负极电极反应为 ;
③ V="67.2" L时,溶液中离子浓度大小关系为 。
(14分)(1)CH4 (g)+CO2 (g)=2CO (g)+2H2 (g) △H="+247.4" kJ·mol-1(2分)
(2)②(2分) 选择CH4不完全燃烧制合成气时,放出热量,同时得到的CO、H2物质的量之比为1∶2,能恰好完全反应合成甲醇(2分)
(3)低温、高压(2分)
(4)①CH4 +2O2 +2KOH=K2CO3+3H2O(2分)
②CH4—8e-+ 9CO32-+3H2O=10HCO3-(2分)
③c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) (2分)
解析试题分析:(1)根据盖斯定律,①×2—③可约去H2O(g),则CH4(g)+CO2 (g)=2CO(g)+2H2(g)的△H=①的△H×2—③的△H=[(+206.2)×2—(+165.0)] kJ·mol-1="+247.4" kJ·mol-1;(2)从能量角度比较,①是吸热反应,需要消耗更多能量,②是放热反应,不需要太多能量;从原子利用率角度,由于CO+2H2→CH3OH,①的产物中氢原子不可能全部变为CH3OH,而②的产物中所有原子都可能全部变为CH3OH;因此选②,甲烷不完全燃烧制合成气时放出热量,还得到物质的量之比为1∶2的CO和H2的混合气体,能恰好完全反应生成甲醇;(3)由于正反应是气态物质体积减小的放热反应,因此采用降低温度、增大压强能使平衡右移,提高CO的转化率,防止催化剂中毒;(4)n(KOH)=2mol/L×2L=4mol,可能先后发生反应①CH4+2O2→CO2+2H2O、②CO2+2KOH=K2CO3+H2O、③K2CO3+CO2+H2O =2KHCO3;当0<V≤44.8 L时,0<n(CH4)≤2mol,则0<n(CO2)≤2mol,只发生反应①②,且KOH过量,则电池总反应式为CH4+2O2+2KOH=K2CO3+3H2O,负极反应式为CH4—8e—+10OH—=CO32—+7H2O;当44.8 L<V≤89.6 L,2mol <n(CH4)≤4mol,则2mol <n(CO2)≤4mol,发生反应①②③,得到K2CO3和KHCO3溶液,则负极反应式为CH4—8e—+ 9CO32—+3H2O =10HCO3—;当V="67.2" L时,n(CH4)=3mol,n(CO2)=3mol,则电池总反应式为3CH4+6O2+4KOH=K2CO3+2KHCO3+7H2O,则得到1mol K2CO3和2mol KHCO3的溶液,则c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)。
考点:考查化学反应运力,涉及运用盖斯定律计算焓变、热化学方程式的书写、评价物质合成方案、影响化学平衡的因素、燃料电池、溶液中离子浓度大小关系等重要考点。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
如下图装置所示,是用氢氧燃料电池B进行的某电解实验:
(1)若电池B使用了亚氨基锂(Li2NH)固体作为储氢材料,其储氢原理是:
Li2NH+H2=LiNH2+LiH ,则下列说法中正确的是 。
| A.Li2NH中N的化合价是-1 |
| B.该反应中H2既是氧化剂又是还原剂 |
| C.Li+和H+的离子半径相等 |
| D.此法储氢和钢瓶储氢的原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某同学设计了如下图所示的装置进行电化学实验,请你根据装置图回答相关问题: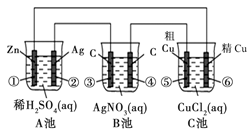
(1)C池属于什么装置 。
(2)电极②上发生电极反应式为 ;B池中发生的总反应方程式为 。
(3)反应进行一段时间后,A、B、C三池中电解质溶液浓度基本不变的是________。
(4)当电路上有0.2 mol电子流过时,电极④上质量变化______g, 电极⑥上质量变化______g。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
科学地补充碘可防止碘缺乏病。
(1)上图为海带制碘的流程图。步骤③的实验操作中用到的玻璃仪器除了烧杯、玻璃棒之外还有 ;当步骤④反应中转移0.2mol电子时生成碘的质量:
(2)碘酸钾(KIO3)是食盐的加碘剂。KIO3在酸性介质中能与H2O2或I-作用均生成单质碘。
请回答下列问题:
①以碘为原料,通过电解制备碘酸钾的实验装置如图所示。电解前,将一定量的精制碘溶于过量氢氧化钾溶液,溶解是发生反应为:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区。电解时,阳极反应: I-+6OH--6e-=IO3-+3H2O,当外电路上通过3mol电子时(碘离子被完全消耗),溶液中的IO3-的物质的量是 ;阴极上产生的气体在标准状况下的体积: 。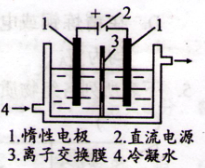
②电解过程中,需通过检验阳极电解液中是否有I-存在以确定电解是否完成。请设计判断电解是否完成的实验方案,并填人下表。仪器不限,可选的试剂:淀粉溶液、H2O2溶液、稀硫酸。
| 实验操作 | 实验现象及结论 |
| | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
Ⅰ.在下图的装置中,属于原电池的是 。
Ⅱ.(1)如图所示,烧杯中为CuCl2溶液,在图中画出必要的连线或装置,使连接后的装置为原电池。电极反应方程式:
铁板: ;碳棒: 。
(2)铜片、锌片连接后浸入稀硫酸中构成原电池,当导线上通过3.01×1022个电子时,锌片质量减少________g。铜片表面析出氢气_________L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)现有如下两个反应:
(A)NaOH + HCl =" NaCl" + H2O (B)2FeCl3 + Cu = 2FeCl2 + CuCl2
①根据两反应本质和特点,判断(A)和(B)分别能否设计成原电池 ;
②如果不能,说明其原因 。
(2)选择适宜的材料和试剂设计一个原电池,电池的总反应为:Zn + CuSO4 = ZnSO4 + Cu,分别写出电池两极的电极反应式,正极 ,负极 。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
【化学与技术】
由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下: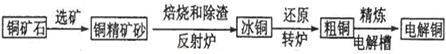
(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转化为低价氧化物。该过程中两个主要反应的化学方程式是 、 ,反射炉内生成炉渣的主要成分是 ;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中将冰铜加熔剂(石英砂)在1200℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式是 、 ;
(3)粗铜的电解精炼如图所示。
在粗铜的电解过程中,粗铜板是图中电极 (填图中的字母);在电极d上发生的电极反应为 ;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为 。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
常见的纽扣电池为Ag Zn电池,它用不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒内靠正极壳一端填充Ag2O和少量石墨组成的正极活性材料,负极盖一端填充Zn
Zn电池,它用不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒内靠正极壳一端填充Ag2O和少量石墨组成的正极活性材料,负极盖一端填充Zn Hg合金作负极的活性材料,电解质溶液为浓KOH溶液。写出此电池的正极和负极反应式以及电池总反应式。
Hg合金作负极的活性材料,电解质溶液为浓KOH溶液。写出此电池的正极和负极反应式以及电池总反应式。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某小分子抗癌药物的分子结构如图所示,下列说法正确的是( )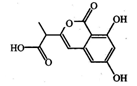
| A.1mol该有机物最多可以和5mol NaOH反应 |
| B.该有机物容易发生加成、取代、中和、消去等反应 |
| C.该有机物遇FeCl3溶液不变色,但可使酸性KMnO4溶液褪色 |
| D.1mol该有机物与浓溴水反应,最多消耗3mol Br2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com