
| A. | NaHA溶液一定呈酸性 | B. | c(H+)•c(OH-)=1×10-14x | ||
| C. | c(Na+)=c(K+) | D. | c(Na+)+c(K+)=0.05 mol/L |
分析 A、NaHA中加一定量的KOH显中性,则NaHA显酸性;
B、水的离子积常数与温度有关,温度越高,水的离子积常数越大;
C、NaHA与KOH恰好反应显碱性,向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性时,NaHA的物质的量应大于氢氧化钾的物质的量;
D、0.1mol/L的NaHA溶液与0.1mol/L KOH溶液混合时,钠离子和钾离子浓度之和不变.
解答 解:A、NaHA中加一定量的KOH显中性,由于KOH为强碱,则NaHA溶液显酸性,故A正确;
B、水的离子积常数与温度有关,温度越高,水的离子积常数越大,温度未知,所以水的离子积常数未知,故B错误;
C、NaHA与KOH恰好反应显碱性,向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性时,NaHA的物质的量应大于氢氧化钾的物质的量,所以同一混合溶液中c(Na+)>c(K+),故C错误;
D、0.1mol/L的NaHA溶液与0.1mol/L KOH溶液混合时,钠离子和钾离子浓度之和不变,则c(Na+)+c(K+)=0.1 mol/L,故D错误;
故选:A.
点评 本题考查了盐溶液酸碱性的判断、溶液中离子浓度的关系等知识点,难度中等,根据影响离子积的因素和电荷守恒、物料守恒来分析解答即可.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
| W | 第二周期中一种非金属元素,第一电离能大于相邻元素 |
| X | 常见的金属,在周期表中的周期序数与族序数相等 |
| Y | 气态氢化物及其最高价氧化物对应的水化物均为强酸 |
| Z | 其原子质量数为56,中子数为30的核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素中有两种元素在第二周期 | |
| B. | W所在主族元素的原子次外层电子数可能为2或8,不可能为18 | |
| C. | X、Y、Z的最高价氧化物对应的水化物两两之间能反应 | |
| D. | 工业上获得X、Y单质的方法主要是电解其熔融的氯化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$ +R3COOH
+R3COOH $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +CH3COOH
+CH3COOH

 ;反应II和IV的目的是保护B中的羟基,防止被酸性高锰酸钾氧化.
;反应II和IV的目的是保护B中的羟基,防止被酸性高锰酸钾氧化.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2 | B. | NO2 | C. | NH3 | D. | NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
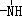 、
、 一定条件下都可以和H+结合.则N4和足量的H+反应生成的粒子的化学式为N4H44+.
一定条件下都可以和H+结合.则N4和足量的H+反应生成的粒子的化学式为N4H44+.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
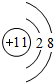 ,C的原子结构示意图是
,C的原子结构示意图是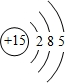 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硼元素、钙元素、铜元素在化学中有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.
硼元素、钙元素、铜元素在化学中有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com