
 +H2O
+H2O| 浓硫酸 |
| △ |
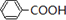 +CH3CH2OH,故答案为:
+CH3CH2OH,故答案为: +H2O
+H2O| 浓硫酸 |
| △ |
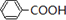 +CH3CH2OH.
+CH3CH2OH.


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
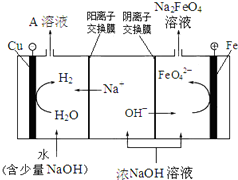 高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂.
高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠和水的反应:Na+H2O=Na++OH-+H2↑ |
| B、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| C、铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| D、氢氧化钡溶液跟稀硫酸反应:Ba2++OH-+H++SO42-=BaSO↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
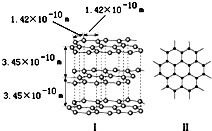 (1)石墨是层状结构,如如图所示.每一层内的碳原子间通过sp2杂化形成
(1)石墨是层状结构,如如图所示.每一层内的碳原子间通过sp2杂化形成查看答案和解析>>
科目:高中化学 来源: 题型:
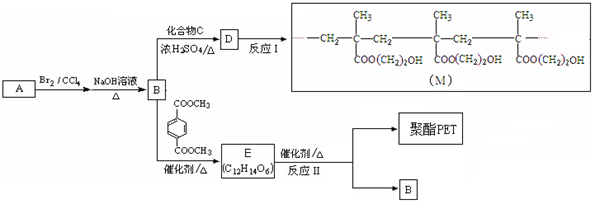
18 |
| 催化剂 |
| △ |
18 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | |
| Y | Z |
| A、元素X和元素Y的最高正化合价相同 |
| B、气态氢化物的热稳定性:H2Y<H2X |
| C、Y2Z2是共价化合物 |
| D、酸性:HZO4>H2YO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
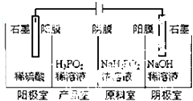 次磷酸(H3PO2)是一种精细化工产品,是一元中强酸,具有较强还原性.
次磷酸(H3PO2)是一种精细化工产品,是一元中强酸,具有较强还原性.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com