
【题目】在KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O反应中,
(1)氧化剂是__,氧化产物是__.
(2)写出该反应的离子方程式.__.
(3)若有219gHCl参加反应,产生Cl2的体积(标况下)为__ L,转移电子__ mol.
(4)Cl2有毒,多余的Cl2通常用氢氧化钠溶液吸收,反应的离子方程式为:__.
【答案】 KClO3 Cl2 ClO3﹣+5Cl﹣+6H+=3Cl2↑+3H2O 67.2 L 5mol Cl2+2OH﹣=ClO﹣+ClO﹣+H2O
【解析】(1)该反应中,氯酸钾中氯元素的化合价由+5价变为0价,所以氯酸钾是氧化剂;HCl中Cl元素化合价由-1价升高到0价被氧化生成![]() ,为氧化产物;正确答案: KClO3 ; Cl2 。
,为氧化产物;正确答案: KClO3 ; Cl2 。
(2)KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O反应中,氯气、水在离子反应中保留化学式,则该反应的离子反应为ClO3﹣+5Cl﹣+6H+=3Cl2↑+3H2O;正确答案:ClO3﹣+5Cl﹣+6H+=3Cl2↑+3H2O。
(3)根据反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O可知,6molHCl参加反应生成氯气3 mol,若有![]() 即
即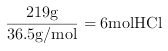 参加反应,则产生
参加反应,则产生![]() 的体积(标况下)为
的体积(标况下)为![]() ,根据
,根据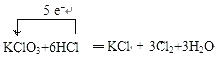 可知转移电子
可知转移电子![]() ,正确答案是:67.2 L ; 5mol。
,正确答案是:67.2 L ; 5mol。
(4)![]() 有毒,多余的
有毒,多余的![]() 通常用氢氧化钠溶液吸收生成氯化钠、次氯酸钠和水,离子方程式为: Cl2+2OH﹣=ClO﹣+ClO﹣+H2O;正确答案: Cl2+2OH﹣=ClO﹣+ClO﹣+H2O。
通常用氢氧化钠溶液吸收生成氯化钠、次氯酸钠和水,离子方程式为: Cl2+2OH﹣=ClO﹣+ClO﹣+H2O;正确答案: Cl2+2OH﹣=ClO﹣+ClO﹣+H2O。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】向1L含0.01molNaAlO2和0.02molNaOH的溶液中缓慢通入二氧化碳,随n(CO2)增大,先后发生三个不同的反应,当0.01mol<n(CO2) ![]() 0.015时发生的反应是:2 NaAlO2+ CO2+2H2O=2Al(OH)3↓+Na2CO3下列对应关系正确的是( )
0.015时发生的反应是:2 NaAlO2+ CO2+2H2O=2Al(OH)3↓+Na2CO3下列对应关系正确的是( )
选项 | n(CO2)/mol | 溶液中离子的物质的量浓度 |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)> c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)> c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)> c(HCO3-)> c(OH-)>c(H+) |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关电解质溶液的说法正确的是
A. 0.1mol·L-1 Na2SO3溶液加水稀释,c(H+)∶c(SO![]() )的值逐渐减小
)的值逐渐减小
B. pH为6的碳酸溶液,水电离出的c(H+)=1.0×10-6mol·L-1
C. pH为12的氢氧化钡溶液与pH为2的盐酸溶液等体积混合,溶液呈碱性
D. 把0.2mol·L-1醋酸与0.1mol·L-1醋酸钠溶液等体积混合c(CH3COOH)+c(CH3COO-)=3c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸甲酯M,常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。M属于芳香族化合物,苯环上只含有一个直支链,能发生加聚反应和水解反应。测得M的摩尔质量为162g·mol-1,只含碳、氢、氧,且原子个数之比为5:5:1。
(1)肉桂酸甲酯的结构简式是______________________。
(2)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如下图所示(图中球与球之间连线表示单键或双键)。G的结构简式为_________________。
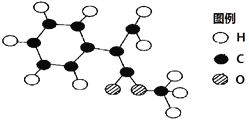
(3)用芳香烃A为原料合成G的路线如下:
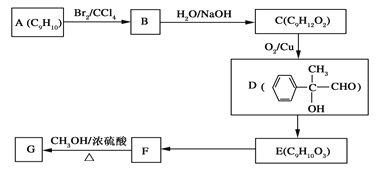
①化合物E中的官能团有________(填名称)。
②E→F的反应类型是________,
F→G的化学方程式为__________________________________________________。
③写出两种符合下列条件的F的稳定的同分异构体的结构简式_________________。
ⅰ.分子内含苯环,且苯环上只有一个支链;
ⅱ.在催化剂作用下,1mol该物质与足量氢气充分反应,最多消耗5mol H2;
ⅲ.它不能发生水解反应,但可以发生银镜反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种物质之间有如下图所示的转化关系: 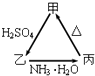
(1)若甲是不溶于水的白色粉末状物质,既能溶于盐酸又能溶于氢氧化钠溶液,则甲是(填化学式). 写出反应的化学方程式
①甲→乙 .
②乙→丙 .
(2)若乙溶液中加入KSCN溶液,有血红色出现,则甲物质是(填化学式).写出反应的离子方程式: ①甲→乙 .
②乙→丙 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是六种短周期的主族元素,原子序数依次增大,A是IA族的非金属元素,B元素的最高价氧化物的水化物与其简单气态氢化物可反应生成盐,C是短周期中原子半径最大的元素,D元素原子L层电子数和M层电子数之差等于B元素最外层电子数,E元素最高正价和最低负价代数和等于4,据此回答下列问题:
(1)F元素在周期表中的位置__________,C原子结构示意图______________。
(2)A、B两元素可形成18电子的分子,该分子的电子式为_______________。
(3)A和氧元素形成的简单化合物,其熔沸点高于A和E形成的简单化合物,原因是____________。
(4)C、D、F可形成复杂化合物C[DF4],该化合物含有的化学键类型为________________。
(5)仅有上述元素形成的化合物或单质间的某些反应,可用以说明E和F两元素非金属性的强弱,写出其中一个离子反应方程式__________________________________。
(6)写出C、D两元素最高价氧化物的水化物反应的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质.请你参与研究并回答下列问题:
(1)甲同学取一束细铜丝用砂纸打磨后在酒精灯上加热至红热,再伸到Cl2的集气瓶中.你认为甲同学在实验中应该观察到的现象是 .
(2)乙同学为验证Fe在冷的浓HNO3中发生钝化但能和热的浓HNO3反应,设计了如图1、2所示的实验,请你指出其中的两处错误:、;纠正上述错误后,请你从绿色化学的角度出发,对图2装置提出改进建议,使装置既能控制反应的进行,又能减少氮氧化物的排放: . 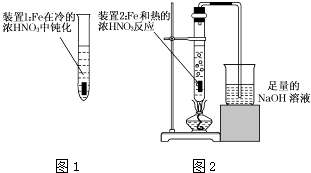
(3)丙同学在Fe和浓HNO3反应后的溶液中加入一块Cu片,Cu片逐渐溶解,反应一段时间后不再溶解(Cu有剩余). ①丙同学依据反应现象得出Cu片溶解的原因是和HNO3发生反应.他依据的反应现象是 .
②丁同学认为丙同学的结论不完全正确.他的理由是 .
(4)请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+ . 说明具体的操作和实验现象 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.用纯碱溶液溶解苯酚:CO32﹣+C6H5OH→C6H5O﹣+HCO3﹣
B.用强碱溶液吸收工业制取硝酸尾气:NO+NO2+2OH﹣═2NO3﹣+H2O
C.用二氧化锰和浓盐酸反应制氯气:MNO2+4HCl(浓) ![]() Mn2++2Cl﹣+Cl2↑+2H2O
Mn2++2Cl﹣+Cl2↑+2H2O
D.向AlCl3溶液中滴加过量的氨水:Al3++4NH3?H2O═AlO2﹣+4NH4++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯醇的结构简式为CH2=CH-CH2OH,它可以发生的反应有:①取代;②加成;③加聚;④氧化;⑤燃烧,其中正确的是
A.只有①②⑤B.只有②③C.除④外D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com