
| 1000ρw |
| M |
| 24 |
| 95 |
| 5.1% | ||
|
| 1000×1.18×20.2% |
| 95 |


科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
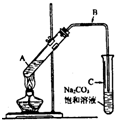 (2009?成都一模)某兴趣小组利用如图装置,取不同浓度的硫酸与 3mL 无水乙醇和 2mL 冰醋酸分别进行制取乙酸乙酯的研究.
(2009?成都一模)某兴趣小组利用如图装置,取不同浓度的硫酸与 3mL 无水乙醇和 2mL 冰醋酸分别进行制取乙酸乙酯的研究. CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O| 组序号 | 催化剂 | 反应现象 | C中饱和碳酸钠溶液中酯层高度 |
| ① | 2mL98%浓硫酸 | 20秒时溶液出现棕色,随反应进行,溶液颜色逐渐加深,最后成黑色;酯层无气泡. | 2.10cm |
| ② | 2mL14mol?L-1硫酸 | 反应后溶液颜色呈棕色,酯层与饱和碳酸钠溶液界面清晰,无气泡. | 2.14cm |
| ③ | 2mL10mol?L-1硫酸 | 反应后溶液颜色呈无色,酯层与饱和碳酸钠溶液界面清晰,无气泡. | 2.16cm |
| ④ | 2mL7mol?L-1硫酸 | 反应后溶液颜色呈无色,酯层与饱和碳酸钠溶液有气泡. | 2.00cm |
| △ |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
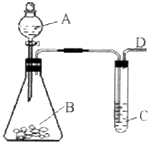 (2009?福州一模)某同学用如图所示的装置来探究SO2的性质及有关实验.
(2009?福州一模)某同学用如图所示的装置来探究SO2的性质及有关实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com